原生代 (大酸化イベントと多細胞生物の祖先) 酸素が満ち、真核生物と多細胞生物が誕生した、生命進化の大転換期 • 約25億〜5.4億年前の時代 • 光合成による酸素の大増加(大酸素イベント)が起こった • 真核生物の誕生(細胞内共生によるミトコンドリア獲得) • 多細胞生物の出現へとつながる進化が進んだ |
 諏訪大社創建の地,前宮の全景風景 |
| 目次 | |
| 1)原生代直前の約24億年前,ヒューロニアン氷期の開始 | |
| 2)太古代から原生代へ | |
| 3)大酸化イベントThe Great Oxidation Event | |
| 4)八硫黄(八員環)の構造 | |
| 5)硫酸還元のプロセス |

地球が史上初めて全球凍結状態(スノーボールアースSnowball Earth)に陥り、生物の大規模な絶滅をもたらした。原因はシアノバクテリアが発生させた膨大な酸素がメタンと反応して水と二酸化炭素に換え、強力な温室効果を持つメタンが激減したことによると見られる。
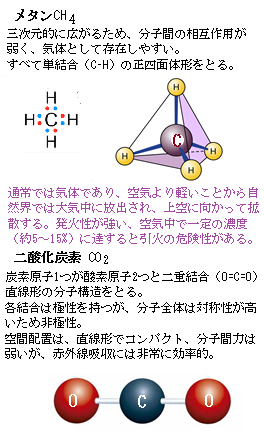
メタンCH4と酸素O2の反応(酸化)の化学式
CH4 + 2O2 ⇒ CO2 + 2H2O
この反応が意味することは、メタンCH4は非常に強力な温室効果ガスで、それが酸素と反応して二酸化炭素CO2(温室効果は弱い)と水H2Oに変わることで、地球の温室効果が大きく低下した。これが 原生代の全球凍結Snowball Earthの一因と考えられている。
 |
| メタンが大気中で約12年しか生き残れない最大の理由は、主に「ヒドロキシルラジカル(OH)」との反応で急速に酸化されてしまうためである。 大気中のヒドロキシルラジカル(OH)による酸化反応は、大気中には「OHラジカル」と呼ばれる非常に反応性の高い分子が存在する。 これはしばしば「大気の洗剤」と呼ばれ、さまざまなガスを分解する。 メタンはこのOHによって連鎖的に酸化される。最終段階まで反応が進み、最終的には CO2 と水 になる。 実際の大気でも、OHラジカルが反応の起点になり、最終酸化までOHが作用する。 ① 開始反応:OHによる水素引き抜き CH4 + OH ⇒ CH3 + H2O ② メチルラジカルの酸素付加 CH3 + O2 ⇒ CH3O2 (メチルジオキシラジカル) ③ 過酸化メチルラジカルの反応(NOがある場合) CH3O2 + NO ⇒ CH3O(メトキシラジカル) + NO2 ④ メトキシラジカルの酸化 CH3O + O2 ⇒ HCHO + HO2 ここで ホルムアルデヒド(HCHO) が生成される。 ⑤ ホルムアルデヒドの酸化 HCHO + OH ⇒ HCO(ホルミルラジカル) + H2O ⑥ ホルミルラジカルの酸化 HCO + O2 ⇒ CO + HO2 ⑦ 一酸化炭素(CO)の最終酸化 CO + OH ⇒ CO2 + H H + O2 ⇒ HO2 上記、段階を経て、最終的に CO2 と H2O になる。 この反応が非常に効率的なため、メタンは 平均12年ほどで大気から除去 される。 大気中のメタンの一部は、土壌中のメタン酸化細菌によって吸収・分解される。 ただし、あくまで大気中のOH反応が主役となる。 メタンは 単純な構造のCH4 で、そのC–H結合は比較的反応しやすい。 CO2の方は、既に「完全に酸化された形」であり、自然界で壊す手段がほとんどない。そのためCO2は100〜200年以上残るのに対し、メタンはほぼ12年と短命になる。 |
メタンが CO2より強力となる科学的メカニズムは、分子構造が複雑で、吸収できる赤外線の種類が多いこともあり、また、メタンCH4は 5つの原子で構成されることで、ねじれ・伸縮・曲げなど、複数の振動モードを持つ。これらの振動が、地球が放出する赤外線の波長とよく一致する。そのため、赤外線を効率よく吸収して熱に変換して閉じ込める。
一方、CO2は直線形で振動モードが限られているため、吸収できる赤外線の種類が少ない。地球が宇宙に放出する赤外線のピークは 10 µm 前後 、メタンの吸収帯はこの領域に近く、効率的に熱に変換するが、CO2の吸収帯は既に飽和気味で、追加のCO2の吸収能力は著しく逓減しやすい。
また、メタンの大気中の濃度が低いため、追加分の効果が大きい。つまり、 CO2は 420 ppm 程度 、メタンは 2 ppm 程度であれば、極めて低濃度であるため、1分子あたりの温室効果の増加量は各段に大きくなる。つまり、濃度が低い赤外線吸収帯が飽和に達していなければ、1分子追加するごとの温室効果の増加量はより大きくなる。これらの要因が合わさり、100年スケールでメタンは CO2の約25倍の温室効果を持つと評価される。
(parts per million【パーツ・パー・ミリオンppm】、つまり、その濃度単位は100万分の1の意となる)
温室効果ガスは、特定の赤外線の波長を吸収する。 しかし、その吸収は、濃度が高くなるほど飽和していく という性質がある。CO2が現在 420 ppmの場合、主吸収帯の15 μm付近では既にかなり吸収されている。追加の CO2 を入れても、吸収が増えるのは『翼(Wing)の部分』だけ となり、1分子あたりの追加効果は小さい。CO2の主吸収帯15 μm付近は、中心(Core)に当たるため吸収が非常に強いが、中心から離れた弱い部分Wingでの吸収能力は、限定的になる。1 ppm 追加しても効果はどんどん小さくなる。そのため 1 分子あたりの追加効果は小さくなる。
メタンは 2 ppm 程度しかないため、中心も翼も飽和に容易に達しない。 逆に追加すると吸収帯全体が強くなる。低濃度ガスは 1 分子あたりの温室効果が大きい 。しかも主吸収帯(7.6 μm付近)は未だ飽和に達していない。追加すると吸収量が丸ごと増える。1 分子あたりの追加効果が大きい。
短期的な気候安定には、メタン削減が非常に効果的だが、.長期的な地球温暖化対策では、CO2削減が不可欠となる。両方とも対策上重要であるが、目的の時間スケールで優先順位が変わる。
太古代末期の約23.3億年前の大酸化イベントでは、好気的環境で安定しない閃ウラン鉱uraniniteによる堆積性ウラン鉱床がこれ以降の岩石から発見されないこと、赤色岩層がこれ以降一般的な堆積岩になること、縞状鉄鉱層が稀になるなど、様々な変化が生じた。しかも、海洋表層水の溶存酸素が深層にも拡大し、嫌気性生物の生息域が大幅に縮小した。
好気的環境とは「酸素が存在し、酸素を利用する生物が活動できる環境」のことであるが、その好気的環境で安定しない閃ウラン鉱uraninite(UO2)とは、「酸素がある場所では化学的に不安定になり、酸化されて別のウラン鉱物へ変質してしまう」という意味である。 つまり、閃ウラン鉱(UO2)は酸素が少ない『還元的環境』でこそ長期間安定して存在できる鉱物だ、ということを示す。
なぜ閃ウラン鉱は好気的環境で不安定なのか?
閃ウラン鉱の主成分は U(IV)=四価ウラン(UO2) である。 しかし、酸素がある環境(好気的環境)では次のように酸化される。
U(IV) → U(VI)
U(VI) は 水に溶けやすい可溶性のウラニルイオン (UO22+) になる。
結果として、閃ウラン鉱は水に溶け出し、二次ウラン鉱物(ウラン酸塩uranateなど)へ変質する。つまり、ウランの溶解性が酸化還元条件に強く依存することが示されている。
ウラン酸塩は、主な種類は、一ウラン酸塩M12UO4、二ウラン酸塩(重ウラン酸塩)M12U2O 、三ウラン酸塩M12U3O、重ウラン酸ナトリウムNa2U2Oなどがあげられる。
ウラン酸塩は、閃ウラン鉱(UO2)が酸化されて U(VI) へ移行した結果として形成されるため、 酸化的環境の指標鉱物として古環境解析に使われる。
酸化帯 → ウラン酸塩(可溶性 U(VI) → 二次鉱物)
還元帯 → 閃ウラン鉱U(IV)が安定
堆積性ウラン鉱床は、ウランが地下水などに溶けて運ばれ、堆積物中の有機物や還元環境によって沈殿・濃集した鉱床を指す。堆積性ウラン鉱床は、花崗岩などに含まれていたウランが地下水や低温熱水に溶け出し、上部の堆積層(礫岩・砂岩・泥岩)に沈殿してできた鉱床である。堆積性は、地表環境の化学条件(酸化・還元)と堆積物の性質が主役という点が特徴で、ウランは酸化状態によって溶けやすさが劇的に変わる元素で、酸化的環境では、6価ウラン(UO22+)として水に溶けやすい。
還元的環境では、 4価ウラン(UO2)として沈殿しやすい。つまり、「酸化帯で溶ける → 還元帯で沈殿する」という化学的スイッチが、堆積性ウラン鉱床の形成そのものを決めている。
花崗岩がウランの供給源で、地下水が花崗岩を通ると、ウランが溶け出す。この際、堆積層の有機物(植物遺体など)が還元剤として働くと、溶けていたウランが沈殿し、ウラン鉱物として固定される。
酸化・還元の境界が鉱床形成の鍵となり、還元的な層では4価ウラン(UO2)鉱物(例:人形石)、やや酸化的な層では6価ウラン(UO22+)鉱物(例:リン灰ウラン石)ができる。代表的な産地は、日本では 岡山県・鳥取県の人形峠が典型例、世界では アメリカ・コロラド州 などに大規模鉱床がある。
地下水が花崗岩をゆっくりと溶かし、ウランを抽出する。この時の地下水は酸化的であることが多い。酸化帯が、ウランが「溶ける」世界で、ウランは酸化状態によって性質が劇的に変わる。酸化帯では、地下水中の酸素がウランをU(IV) → U(VI) に酸化し、ウラニルイオン(UO22+)として水に溶けて運ばれる。酸化帯は「ウランを溶かして運ぶコンベアベルト」のような役割を果たす。
酸化帯で溶けたウランは、地下水の流れに乗って堆積層の中を移動する。礫岩・砂岩など透水性の高い層は流れやすい。地下水の流路は、古い河川堆積物の中をくねりながら進む。その先にウランが「沈殿する」世界「還元帯」が待っている。
還元帯とは、酸素が乏しく、電子を与える物質(有機物や硫化物など)が豊富な環境である。植物遺体などの有機物や黄鉄鉱(Fe2+を含む硫化鉄)、泥質堆積物が地下水中のウランU(VI)をU(IV) に還元する。すると、これがウラン鉱物(人形石、閃ウラン鉱など)として堆積する。
(閃ウラン鉱は、二酸化ウラン UO2から成る立方晶系鉱物。黒色の亜金属光沢がある。少量のトリウム・鉛などを伴い、強い放射能をもつ。熱水鉱床やペグマタイトpegmatiteなどに産するウランの主要な鉱石鉱物である..。
ペグマタイトは、数 cm〜数 mの大きな結晶が、ぎっしり詰まった火成岩、主に花崗岩のマグマの『最後のしずく』からできる岩石。マグマは、冷えるにつれて普通の成分から先に固まる。花崗岩マグマを例にすると、斜長石・カリ長石・石英といったメインの成分が、温度が下がるにつれて次々に結晶化する。
普通の成分が結晶として抜けていくと、液体部分には、水・フッ素・リチウム・ベリリウム・ベリリウム・ウラン・トリウムなど、揮発性成分や希元素がどんどん濃縮されていく。これが、マグマの『最後のしずく』と呼ばれる。
花崗岩質のものが多いため巨晶花崗岩【きょしょうかこうがん】あるいは鬼御影【おにみかげ】と呼ばれることもあるが、閃緑岩質や斑糲岩質のものもある。岩脈などに小岩体として産出する。)
目次へ
原生代早期の約22.29億年前、地球上に現存する最古の隕石痕であるヤラババ・インパクトの衝突構造は、西オーストラリアの イラガーン・クラトンYilgarn Cratonに位置し、地球最古級の「太古代クラトンArchean craton」として世界的に認められている。西オーストラリアの大部分を占める巨大な安定地塊であり、ジャックヒルズJack Hillsで発見されたジルコンzirconは、約44億年前〜42.7億年前の地球最古級を示す。ジルコンは、化学式 ZrSiO4をもつ「ジルコニウムZrのケイ酸塩鉱物」で、極めて安定し壊れにくいことから、地球最古の鉱物として知られている。宝石としても利用され、地質学では年代測定のタイムカプセルとして重要な役割を果たす。これにより、地球の最初期(冥王代〜始生代初期)の地殻が残っていることを示した。その上で起きた隕石の衝突であった。
(ジルコンには微量のウランUやトリウムThを取り込む。それが放射壊変して鉛(Pb)に変わる性質を利用して年代を測る【U-Pb年代測定】)
クレーターは風化・浸食を受けているが、元の直径は約30〜70kmと推定されている。厚さ2〜5kmの氷床を伴う花崗岩質の地殻に落下した場合、最大 5000億tの氷が瞬時に昇華したと推計されている。
衝突年代が、地球が全球凍結状態Snowball Earthから脱し始めた時期と一致するため、 衝突が氷床を融解させ、気候変動を引き起こした可能性 が指摘されているが、「ヤラババ衝突が氷期を終わらせた」と断定できる段階ではない。
クレーターの正確な形状・規模は、侵食が極めて進んでいるため、地表にはほとんど痕跡が残っていない。地下構造の詳細は、今後の地球物理探査に期待されている。また、具体的な隕石の組成も、まだ特定されていない。
ヒューロニアン氷期(約24~22億年前)は、シアノバクテリアが光合成で酸素を放出したことにより、大気中の温室効果ガス(特にメタン)が酸化されて激減し、地球が急激に寒冷化したと考えられている。メタンの酸化は温室効果を大幅に弱め、氷期の引き金になったと最新研究でも説明されている。
ヒューロニアン氷期は、大酸化イベントGreat Oxidation Event(GOE) とほぼ同時期に起きた。 その中心的な駆動力が シアノバクテリアの酸素発生型光合成 であった。
シアノバクテリアは光合成により、大量の CO2を有機物として固定する。そのため、大気中の CO2濃度が低下し温室効果が弱まり、寒冷化が進む。
光合成による CO2の直接消費は、シアノバクテリアは次の反応で CO2を固定する。
CO2 + H2O ⇒ CH2O(ホルムアルデヒド)+O2
大量の CO2が有機物として固定されれ、大気中の CO2濃度が低下し、温室効果が弱まり、寒冷化が進む。
(シアノバクテリアが光合成の途中で一瞬だけ生み出すホルムアルデヒドCH2Oは、毒性のある中間体であり、細胞はすぐに別の代謝物へ変換して利用または無害化する。 つまり、ホルムアルデヒドは「最終産物」ではなく、「炭素固定の通過点として瞬間的に現れるだけの物質」である。その「高速解毒」は、光合成生物に共通する安全装置として働く。
ホルムアルデヒドは、化学分野の基本的な構成要素であり、様々な産業および家庭用用途で重要な役割を果たしている。この無色で刺激臭のあるガスは、多くの製品の製造に不可欠であるだけでなく、環境中にも自然に発生する。ホルムアルデヒドは広く使用され存在しているにもかかわらず、潜在的な健康への影響、特に発癌性のために大きな懸念事項となっている。)
上記に伴い放出された O2がメタンCH4を急速に酸化し、二酸化炭素と水に変える。そのため酸素の増加がメタンの酸化を通して温室効果を弱めた。
メタンの酸化反応 CH4 + 2O2 ⇒ CO2 + 2H2O
シアノバクテリアが放出した O2は、海洋表層に蓄積し、嫌気性のメタン生成菌を殺す。これにより メタンの生産量そのものが激減した。 つまり、 「メタンの供給が減り、残ったメタンも酸化される」 という二重の効果で、メタンがほぼ消滅したと考えられる。
この反応の重要性は、メタンが CO2の 20〜30倍以上 の温室効果を持つ 。そのメタンが酸素によって急速に減少し、結果として地球の温室効果が劇的に弱まった。氷床が拡大し、氷期が暴走(ice–albedo feedback) したと考えられる。
 シアノバクテリアは、光エネルギーを、光化学系II(PSII)→光化学系I(PSI)の二段階で受け取り、電子を水から引き抜いて酸素を発生させ、その電子エネルギーをCO2 の固定に使うATP と NADPH に変換する。これは植物と同じ酸素発生型光合成の仕組みでもある。
シアノバクテリアは、光エネルギーを、光化学系II(PSII)→光化学系I(PSI)の二段階で受け取り、電子を水から引き抜いて酸素を発生させ、その電子エネルギーをCO2 の固定に使うATP と NADPH に変換する。これは植物と同じ酸素発生型光合成の仕組みでもある。シアノバクテリアは フィコビリソームphycobilisome という色素タンパク複合体で光を効率よく吸収する。吸収した光エネルギーを 光化学系II(PSII) と 光化学系I(PSI) に渡す。そのため光環境(光量・波長の変化)に適応する光獲得戦略が重要となる。
光エネルギーを受け取った PSII は、次の反応を起こす。水を分解して 酸素O2を放出し電子(e⁻)を取り出し、電子伝達系へ送る。これが 酸素発生型光合成の核心で、シアノバクテリアが植物と同じ酸素発生型光合成を行うことが強調さる。
光化学系II(PSII)は、水を分解し、電子を取り出すことで光エネルギーを受け取った PSII は、次の反応を起こす。
2H2O ⇒ O2 + 4H+ + 4e-
水を分解して 酸素O2 を放出し 電子e⁻を取り出し、電子伝達系へ送る。これが 酸素発生型光合成の核心になる。シアノバクテリアが植物と同じ酸素発生型光合成を行うことが知られる。
電子伝達系では、光エネルギーを ATP に変換する。PSII から取り出した電子は、膜内の電子伝達鎖を流れる。 電子が流れるとき、膜を隔てて プロトン濃度差(H+勾配) が生じる 。その勾配を利用して ATP 合成酵素が ATP を作る。これは光リン酸化と呼ぶ。
PSI は光を受けて電子を再び高エネルギー状態に引き上げる。 その電子を使って、NADPH(還元力)を生成する。
NADP+ + 2e- + H+ ⇒ NADPH
光反応で作られたNADPHとATP が、後に CO2固定に使われる。
暗反応(カルビン回路)では、CO2を糖に変換する。
光反応で作られた ATP と NADPH を使い、CO2を固定する。
CO2 ⇒ CH2O
光反応と暗反応の両方がシアノバクテリアの基本代謝となる。
約22億年前、ヒューロニアン氷期の終了までの生物
氷期の間に大気中へ放出された二酸化炭素が消費されず、温室効果を引き起こしてアイス・アルベド・フィードバックIce-albedo feedbackを突破して解氷を始める。言わば、正のアイス・アルベド・フィードバックで、氷や雪が減ることで地表の反射率albedoが下がり、より多くの太陽エネルギーが吸収され、さらに温暖化が加速する。 そのヒューロニアン氷期に CO2を大量に排出した最大の要因は、火山活動による。氷期中でもプレート運動と火山活動は止まらず、 数千万〜数億年スケールで CO2が大気に蓄積した。一方、氷に覆われた地球では、 風化作用がほぼ停止し CO2を吸収するプロセスが止まった。 火山だけが CO2を供給し続ける。その結果、CO2がゆっくりと増加した。温室効果が回復して氷期が終わるも、氷期中のCO2を吸収する風化が止まったまま、火山性 CO2が大気に蓄積し続け、最終的に氷期を終わらせたと考えられている。
(氷床が大陸のほぼ全域覆うと、岩石が露出している部分がほとんどなくなる 。河川も止まり、雨もほぼ降らない、極端に乾燥した世界になる。
化学風化とは、
雨水H2O+CO2 → 炭酸H2CO3→ 岩石の溶解 → 海へ → 炭酸塩として固定 というプロセス
実際にはこの反応は完全に右へ進むわけではなく、 CO2(aq) と H2CO3は平衡状態にある。
CO2(aq) + H2O ⇔ H2CO3 【CO2(aq) は、水に溶けた状態の二酸化炭素を示す化学表記。aqueous=水溶液中】
そして炭酸は弱酸なので、さらに部分的に電離して
H2CO3 ⇔ H+ + HCO3- ⇔
HCO3- ⇔ H+ + CO32-
この一連の反応が、 岩石を溶かし、炭酸塩として炭素を固定する風化作用の基盤になる。
これが氷に覆われた大陸であれば、雨が降らない、氷床の上では風化が起きない、氷の下の岩石は水に触れない、河川がないため溶けた物質が海へ運ばれない 。
CO2を吸収する地球の炭素シンクcarbon sinkがほぼゼロになる。
つまり、大気中の CO2を吸収し、長期間にわたって地球のどこかにしまい込む仕組みや場所、『炭素が大気から消えていく貯蔵庫』 が存在しない状態を言う。)
正のアイス・アルベド・フィードバックでは、地球上の雪氷面積が小さくなると、太陽光に対する反射率albedoが低下するために、より多くの熱を吸収することで陸や海が暖められ、雪氷面積がさらに小さくなる。地球の気候変動を支配する重要なメカニズムの一つとして考えられている。また、河川熱流入によって北極海の海氷縁が後退することで、海面への太陽光吸収量が増加し、さらなる海氷融解や海水温上昇が促進される。
原生代初期のヒューロニアン氷期(約24〜21億年前)は、地球史上初の「ほぼ全球凍結」に近い深刻な氷期だったと考えられている。この時期、嫌気性生物や初期のシアノバクテリアの多くが絶滅したと推定されている。それでも生命は完全には絶えなかったのは、「避難所refugia」の存在が考えられている【ラテン語の「fugere」(逃げる)と「re-」(再び)から構成されている】。
氷が完全に地球を覆うわけではなく、海氷の割れ目や風で開いた海面・開水域polynyaなどが局所的に存在し、光も届き、光合成生物が生き残れた可能性が存在した。深海の熱水噴出孔は、高温や化学エネルギーを提供し、嫌気性微生物が生き残るための「温水域」になりえた。氷期の前から存在していた生命の多くは化学合成生物だったため、光がなくても生存が可能であった。また、生物は火山の付近のような熱水活動のある場や低緯度海域で生存していたと見られる。
氷床下の海は、氷が厚くても、海水は完全には凍らない。氷床下に液体の海が維持される。現代の南極でも同じ仕組みの湖や海が存在しており、そこに微生物が生き続けている。岩石の割れ目など地下の微生物圏に住む微生物は、放射線分解や化学反応などからエネルギーを得て生きることができる。氷期の影響をほとんど受けないため、「地下の微生物圏」になっていたと考えられている。
放射線が水や鉱物を分解し、化学エネルギー源を生み出す。放射線(主にウラン・トリウム・カリウムの自然放射線)が岩石中の水に当たると、水素H2や酸化剤(硝酸塩、硫酸塩、過酸化物など)が生成される。これらが、微生物にとって『食料』になる。特に放射線分解で生まれた水素は、地下微生物にとって最も重要なエネルギー源となる。多くの地下生物は、電子供与体としてH2や、電子受容体として硫酸塩・硝酸塩・二酸化炭素を使って代謝を行う。これは、地表の光合成に相当する「地下の化学合成」で、放射線分解が微生物代謝を支える可能性が指摘されている。
放射線は岩石中の鉱物にも作用し、鉄・硫黄・炭素などの化学状態を変化させる。これにより、鉄酸化細菌・硫黄酸化細菌・メタン生成菌などが利用できる化学エネルギーが供給される。つまり、『岩石+放射線+水 → 生命の燃料』という仕組みが地下で成立している。しかも、放射線に強い微生物は、DNA修復能力が極めて高い。放射線はDNAを傷つけるが、放射線耐性微生物は驚異的な修復能力を持っている。また、真核生物の一部が極めて高い放射線耐性を持つことが示されている。そのDNAを高速で修復する酵素群や酸化ストレスを抑える抗酸化物質、乾燥耐性などが生命維持を支えている。
鍾乳洞に暮らす生物は、光のない・栄養の乏しい・温度変化が少ないという極端な環境に適応し、独特の進化troglomorphicを遂げている。特に湿度の安定性が生存の鍵で、洞窟の深部ほど特殊化した生物が見られる。鍾乳洞という極限環境は、 完全な暗闇で光合成が不可能、視覚の退化が進む、栄養が極端に乏しい、それでも外部から運ばれる有機物や微生物が主なエネルギー源となる。
洞窟の生態系の根幹には微生物がいる。光のない洞窟で一次生産者として重要な化学合成細菌は、硫黄・鉄・マンガンなどを酸化してエネルギーを得る。化学合成細菌などが、壁面に微生物マット(バイオフィルムbiofilm)を形成し、他の生物の餌となる。洞窟魚やヨコエビなどの洞窟生物は、この微生物マットを直接・間接に利用して生きている。バイオフィルム内には、細菌・真菌・藻類・原生生物などが混在し、三次元的に分布する。この『自前の家』を作る微生物が分泌する粘着性の菌体外多糖(EPS)やタンパク質、そしてDNA が膜を形成し、内部を包む。EPS が外界の刺激から内部の微生物を守る防壁になる。
バイオフィルム内部は酸素濃度が低いが、偏性嫌気性菌が多く生息し、外部とは異なる代謝活性や特性を示す。微生物が有機物を分解し、栄養塩を再循環する。この岩石表面のバイオフィルムが、洞窟魚やヨコエビ、貝類などの洞窟生物の餌になる。
白く透明な体で水中の微生物や有機物を食べるヨコエビや、長い脚や触角で空間を把握し、捕食者として洞窟生態系の上位に位置する洞窟クモ・ムカデなどの糞は洞窟の重要な栄養源となり、昆虫や微生物群集を支える。
硫黄洞窟や火山洞窟は特に多様であるが、温度・湿度が安定し、特に湿度は洞窟生物の生存に決定的な要因となり、その隔離環境に適応して、独自の進化を遂げている。
目次へ
ヒューロニアン氷期は、生物大量絶滅を引き起こしたが、その後、地球は大きく変わる。ヒューロニアン氷期は「大酸化イベントThe Great Oxidation Event(GOE)」と重なる。大気中の酸素が急増し、酸素を利用できる生物(好気性生物)が台頭した。酸素呼吸はエネルギー効率が高いため、生命の活動範囲が大きく広がった。
酸素呼吸が生命の活動範囲を劇的に広げた理由は、一言でいえば 「桁違いのエネルギー密度を手に入れたから」 である。生命はエネルギーを得るためには、栄養分(糖など)から電子を取り出し、どこかに渡す必要がある。酸素なしの嫌気呼吸では、電子の受け取り手が弱い(硫酸塩、硝酸塩など) ので.取り出せるエネルギーが少ない 。
酸素ありの好気呼吸では、 酸素は電子を強力に引きつける(電気陰性度が高い)。酸素は還元されると莫大なエネルギーが放出される。その結果、 1分子のブドウ糖から得られるATP量は約18倍に跳ね上がる (嫌気呼吸は2ATP、好気呼吸は最大38ATP)。このため、酸素が増えると環境全体が 「高エネルギーの電子受容体が豊富な世界」 へと変わった。
真核生物の進化を考えるキーとなる現象の一つに細胞共生endosymbiosisがある。細胞共生とはある生物の細胞が他の生物の細胞内に入り込んで(取り込まれて)一体となって生活することにある。この現象が生物進化、特に真核光合成生物の進化と多様性の実現に大きな役割を果たしてきた。ミトコンドリアの構造は、細胞共生で酸素が増えたことで、ある細菌(祖先はプロテオバクテリア)が 酸素呼吸の達人 として進化した。2021年に正式名称がプセウドモナドータ Pseudomonadota(シュードモナドータ門)に改名されたため、現在の分類学では「Proteobacteria プロテオバクテリア」という名前は旧称として扱われている。 そして、別の細胞(古細菌系の祖先)がこの細菌を取り込み、 共生関係を築いた。
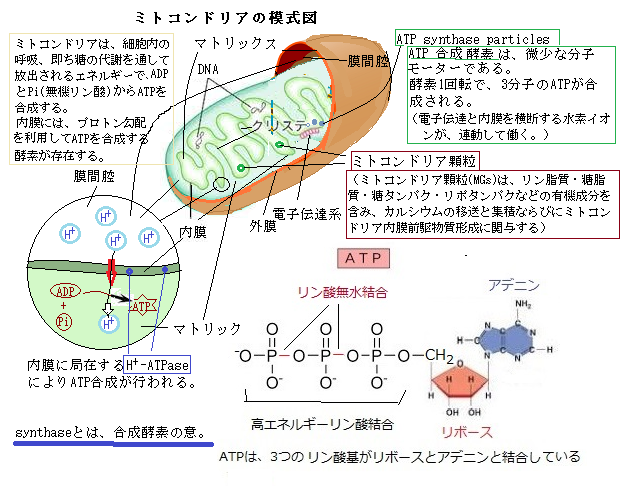 地球上で最も多様な細菌群の一つで、海・土壌・動植物の体内・深海・極限環境などあらゆる場所に生息 • 大腸菌、サルモネラ、ビブリオ、ヘリコバクターなど、医学的に重要な種も多数含む
• 光合成・化学合成・窒素固定・嫌気呼吸など、代謝の多様性が極めて高い
地球上で最も多様な細菌群の一つで、海・土壌・動植物の体内・深海・極限環境などあらゆる場所に生息 • 大腸菌、サルモネラ、ビブリオ、ヘリコバクターなど、医学的に重要な種も多数含む
• 光合成・化学合成・窒素固定・嫌気呼吸など、代謝の多様性が極めて高い取り込まれた細菌は膜を二重に持つ。.現在のミトコンドリアが二重膜なのはこの名残である。取り込まれた細菌は、ATPを大量に生産できた。宿主細胞は『外部エンジン』を手に入れた。宿主は取り込む細菌を消化せず、栄養と保護を提供して、相利共生が成立した。この構造的な安定性が、ミトコンドリアの起源あった。
真核細胞の複雑さは、エネルギーの爆発的増加によって支えられている。 ミトコンドリアを持つことで、細胞は次のような構造を維持できるようになった。細胞骨格(アクチン・微小管) なしでは、大量のATPを消費するため、ミトコンドリアなしでは維持困難であった。膜構造の複雑化(核膜・小胞体・ゴルジ体) は、 膜輸送やタンパク質加工はエネルギーを大量に使う。DNAの巨大化と複雑な制御には、遺伝子の転写・翻訳・修飾はATPを大量に必要とする。また、細胞内区画化compartmentにより代謝経路を分離し、効率化できた。
つまり、 ミトコンドリアはエネルギーの発電所であるばかりか、複雑な細胞構造を支える基盤そのものとなった。
酸素 → ミトコンドリア → 真核生物 → 多細胞化 の連鎖 酸素増加は、次のような進化の階段を登って行った。
1. 酸素が増える 。2. 酸素呼吸が高効率化。 3. 酸素呼吸細菌が誕生。4. それを取り込んだ細胞がミトコンドリアを獲得した。 5. エネルギーが爆発的に増え、複雑な細胞構造の維持が可能になった。 6. 真核生物が誕生した。 7. 多細胞化・大型化・高度な生態的ニッチの開拓へ 、この連鎖は、地球生命史の中でも最も劇的な構造改革であった。
酸素が複雑な細胞を可能にした構造的理由は、酸素は最強の電子受容体で、莫大なエネルギーを生む。そのエネルギーを使う細菌が進化 • その細菌が宿主細胞に取り込まれた。そのミトコンドリアに、ミトコンドリアが大量のATPを供給し、高エネルギーを必要とする複雑な細胞構造(核・細胞骨格・膜系)が維持可能になった。結果として真核生物と多細胞生物が誕生した。
「複雑な生命」を支える燃料になる高エネルギーが増えると、生命は、大型化(細胞・個体など) • 高度な運動(筋肉活動) • 長距離移動 • 神経系の発達(脳は大量のATPを消費) • 多細胞化と組織分化に伴う相互連携 • 高い代謝速度(恒温動物など)など 、つまり、酸素呼吸は 生命の構造・行動・生態的ニッチecological nicheを爆発的に拡張した。生態的ニッチは、 「その生物が世界の中でどんな役割を担い、どんな条件で生きているかをまとめた概念」 と考えられる。その生態的ニッチの核心 は、『どんな環境条件で生きられるか』、『何を食べ、誰に食べられるか』、『どんな行動・生理・形態で生きているか 』など生命活動の根源であれば、酸素呼吸はエネルギー効率が極めて高いため、利用できるニッチが爆発的に増大した。つまり、酸素呼吸は 「多細胞化・大型化・代謝のの加速化など生態的ニッチの多様性と拡大を可能にする最高質のエンジン」 の獲得を意味した。
氷期の原因をつくった張本人でもあるシアノバクテリアは、ヒューロニアン氷期後の原生代前期に再び繁栄した。彼らは酸素を大量に生み出し、海洋の生態系の基盤となり続けた。
その氷期の後の原生代前期~中期の約21〜18億年前には、後の多細胞生物の祖先・真核生物(核を持つ細胞)が出現し増加した。酸素の増加が、ミトコンドリアの進化と複雑な細胞構造の構築を可能にした。これが後の多細胞生物の進化の前提条件となった。
氷期前の嫌気性生物中心の世界から、氷期後は 酸素世界に適応した生物が主役となり、地球の生態系が根本的に変わった。ヒューロニアン氷期は、生命を一度ふるいにかけ、酸素世界に適応する生命が台頭する転換期となった。
これは、真核生物の起源と酸素濃度の上昇が同期していることを示している。大酸化イベント(GOE)で大気中の酸素が上昇したが、海洋はしばらく鉄や硫黄により還元的なままであったため、海の中には酸素をすぐに消してしまうほど巨大な『還元物質の貯蔵庫』であった。つまり海は鉄と硫黄の『酸素吸収分子』で満ちていた。GOE 以前の海は、溶存還元鉄(鉄の二価イオンFe2+)や溶存硫化物(硫化水素イオンHS⁻)が大量に溶け込んだ強還元的な海であった。これらは酸素と出会うとすぐに還元して沈殿した。
Fe2++ O2→ 三価鉄の酸化物Fe2O3
(赤鉄鉱・ヘマタイトの化学式としてFe2O3 が示されている。これにより形成されたのが縞状鉄鉱層であり、現在工業的に使われる鉄鉱石の大半がこの縞状鉄鉱層から採掘されている。)
原生代前期(約25〜16億年前)において、硫化水素イオンHS- が大量に溶け込んだ強還元的な『硫化物海』だった」と考えられている。 ただし、重要なのは どの海域でも一様にそうだったわけではない、という点で、ここに原生代前期のダイナミズムが潜んでいる。
ただ、基本的には、強還元的で HS⁻ が豊富で、大気中の酸素はまだ極めて低濃度であり、海洋深部は酸素が届かず、鉄Fe2+と硫化物HS⁻が豊富で、海底火山からの熱水活動から硫化水素H2S が大量供給され、pH 7〜8 の海水では H2S の多くが 強還元的なHS⁻ (溶存硫化物)として存在した。深海も HS⁻に富む還元的環境が一般的であった。
化学平衡は、 H2S ⇔ HS⁻ + H2
浅海では局所的に酸化環境が生まれた。シアノバクテリアの光合成により、沿岸・表層では 微量の O2が局所的に蓄積し、.その結果、浅海では HS⁻ が酸化される、 HS⁻ + 2O2 → 硫酸塩SO₄²⁻ + H+ の酸化が進行し、.酸化フロントが形成された。
この酸化フロントで起きた反応により、深海=硫化物海HS⁻、浅海=局所的に酸化され硫酸塩SO₄²⁻が生成 という二層構造が成立していたと考えられている。
やがて、酸化フロントでの
HS⁻ → SO₄²⁻ の酸化が進行が進み、
その結果、硫酸塩SO₄²⁻ 濃度が徐々に上昇し、硫酸塩還元が地球規模で始まった。
Fe2+が豊富な深海 + 酸化フロントで Fe2+が酸化 → Fe(III)の沈殿
Fe2++ O2→ 三価鉄の酸化物Fe2O3
これが縞状鉄鉱層Banded Iron Formation(BIF) の形成に寄与、つまり、 深海の還元性(HS⁻・Fe2+)と浅海の酸化性(O2)との境界が BIF を生んだ という構図でとなった。
微生物による硫酸還元
硫酸還元微生物は、硫酸塩SO42-を最終電子受容体として利用し、硫化水素H2Sを生成する微生物であり、環境中で重要な役割を果たしている。
硫酸還元微生物Sulfate-Reducing Microorganisms(SRM)には、硫酸還元細菌Sulfate-Reducing Bacteria(SRB)と硫酸還元古細菌ulfate-Reducing Archaea(SRA)からなるグループで、硫酸塩SO42-を電子受容体として利用し、これを硫化水素H2Sに還元する。これらの微生物は、呼吸可能な酸素O2が存在しない嫌気性環境で主に活動し、硫酸をエネルギー源として利用する。嫌気性環境は、酸素分子が互いに結合してO2を形成することを困難にする条件を示す。代わりに、酸素Oは他の分子と結合して硝酸塩NO3や硫化物SO3などの化合物を作る。硫酸還元微生物は、地球上で最も古い微生物の一つと考えられ、太古代中期の35億年前から存在しているとされている。
(sulfate;硫酸塩。Microorganisms(微生物)とは、『目に見えないほど小さな生物』という広い概念。ただ、分類学的な単位ではない。細菌Bacteriaや古細菌Archaea(アーキア)、そして真核生物Eukaryotesの一部(酵母・カビ・原生生物)など 、つまり、Microorganisms は「生活様式による呼び名」であり、 Bacteria と Archaea は「系統進化上のドメイン」である。
Bacteria(細菌)は、地球上で最も多様で、最も研究されている原核生物であり、 シアノバクテリアによる 大酸化イベント(GOE) • 硫酸還元細菌(SRB)による堆積物の硫黄循環 • 窒素固定の起源でもある。原核生物は核膜を持たず単純な細胞構造を持つ一方、真核生物は核膜や膜で囲まれた細胞小器官を複数持つ複雑な構造体である点で大きく異なる。
Archaea(古細菌) は、見た目は細菌に似ているが、分子レベルでも、別の生命世界を示す。 細胞膜は、エーテル結合脂質(イソプレノイド鎖) で、高温・高塩・高圧に強い。真正細菌の細胞膜の外側に層を形成する細胞壁の主要物質であるペプチドグリカンPeptidoglycan構造の細胞壁を持たないが、遺伝子発現の仕組みがRNAポリメラーゼ・ヒストン様タンパク質など、真核生物に近い →極限環境に強い(高温泉、深海熱水、酸性湖などが生息環境に適応)。
二酸化炭素と水素を原料としてメタンを合成する技術(メタノジェネシスMetagenesis)は Archaea のみが備え、初期地球の嫌気的生態系の中心 • 深海堆積物や海底下生命圏の主要構成員として適応した。特に 硫酸還元古細菌(SRA)は、超高温の海底熱水環境で進化し、細胞膜・酵素・代謝系の三位一体の仕組みによって 80–110 °C という高温でも安定して生命活動を維持する。特にエーテル結合脂質phytanyl ether lipidsを持つ膜は、高温環境で重要で、一般的な細菌のエステル結合脂質より熱に強く、これにより、100 °C 近い熱水環境でも膜流動性を安定化し加水分解されにくい。
古細菌のエーテル結合脂質archaeal ether lipidsを、化学式・部分構造式を含めて構造式は、
1. 基本単位は、フィタニル基phytanyl group(C20H42)
古細菌の膜脂質の疎水鎖は、脂肪酸ではなく イソプレノイド鎖であり、その代表が フィタニル基(C20H42)。
フィタニル基の部分構造(イソプレノイド 4単位)
CH3–CH2–CH(CH3)–CH2–CH(CH3)–CH2–CH(CH3)–CH2–CH(CH3)–CH3
4つのイソプレノイド単位が連結 (イソプレノイドは、基本単位であるイソプレンC5H8が直列に結合した構造を持っている。イソプレンは、5つの炭素原子と8つの水素原子から成る化合物で、これが2つ以上結合することで、モノテルペン(C10)、セスキテルペン(C15)、ジテルペン(C20)などの異なる種類のテルペノイドが形成される。
多くの分岐メチル基(–CH3)があり、熱に強い剛直な鎖になる 。
2. Archaeol(ジフィタニルグリセロールジエーテル)の構造式
古細菌膜の基本骨格は archaeol で、化学式 C40H82O3(頭部を除く)
構造式の極性頭部は、R–O–PO32- など
│ HO–CH2–CH(OH)–CH2–O– (フィタニル基 C20)
│ O–(フィタニル基 C20)
- グリセロール骨格は sn-2,3 配置(細菌とは鏡像) 、結合は エーテル結合(–O–CH2–)
- 疎水鎖は フィタニル基 (C20H42)×2
3. GDGT(テトラエーテル脂質)の構造式
超好熱性古細菌が持つ 単層膜の主成分が グリセロール.ジアルキル.グリセロール.テトラエーテル glycerol dialkyl glycerol tetraethers(GDGT)
化学式(基本形) C86H174O6(環構造なしの場合)
構造式(図として表現)
親水頭部–O–CH2–CH(OH)–CH2–O–[C40 イソプレノイド鎖]–O–CH2–CH(OH)–CH2–O–親水頭部
特徴 - C40のイソプレノイド鎖が左右のグリセロールを橋渡し、これが膜を 単層monolayerにする ので、高温で膜が溶けたり剥がれたりしない。
4. 代表的な頭部基(R)の化学式
古細菌の極性頭部は多様で、代表例を挙げると
硫酸還元古細菌Archaeoglobusでは、 PI・PG(ホスホグリセロール)系が多いことが知られている。
5. Archaeol の“ほぼ完全な構造式”を文章で描く
R–O–PO32- R は極性頭部(例:イノシトール、グリセロールなど)
│ HO–CH2–CH(OH)–CH2–O–CH2–(C20H41)
│ O–CH2–(C20H41) (C20H41) がフィタニル基
硫酸還元古細菌における意義 硫酸還元古細菌(Archaeoglobus)は 80–110 °C の熱水環境で生きるため、
- エーテル結合 → 加水分解されにくい - イソプレノイド鎖 → 熱で折れにくい - テトラエーテル単層膜 → 膜が溶けない という三重の耐熱構造が必須となった。
典型的な水素資化性メタン生成アーキアの主反応は CO2 + 4H2 ⇒ CH4 + 2H2O
ここで必要なのは 分子状水素 H2 であって、水そのものではない。メタン生成アーキアは「水を電気分解のように割って水素を取り出す」能力は持っている。
高温・高塩・高圧という条件は、むしろメタン生成アーキアにとって好環境であって、
高温 - 超好熱性メタン生成アーキアは、80–100℃ 以上でも増殖でき、温度依存性を考慮したメタン生成の研究も進んでいる。
高圧 - 50 bar 程度までの高圧下で、CO2 + H2 → CH4 を行う「高圧メタン細胞ファクトリー」としての利用が検討されている。
高塩 - 高塩環境に適応したメタン生成アーキアも知られており、塩濃度に応じて代謝や膜構造を調整している。
つまり、「高温・高塩・高圧」だからこそ、CO2 + H2 → CH4 型のメタン生成はむしろやりやすい場合がある。
真核生物は、生命の三大ドメインのひとつで、細胞内に 核 を持つ生物すべてを含む巨大なグループで、 含まれるものは、 動物 • 植物 • 菌類(カビ・キノコ・酵母) • 原生生物Protistsなど、 つまり、真核生物は「上位の大分類」であり、 原生生物もその中の一部である。
原生生物Protistsは、真核生物のうち、 動物でも植物でも菌類でもないものをまとめた『便宜的なグループ』で、単細胞が多い(多細胞の例もある) が、代謝・生活史が非常に多様で、しかも系統的にはバラバラ、つまり単系統ではない。ミドリムシ・ アメーバ・ゾウリムシ・藻類(緑藻・褐藻・紅藻の一部)・粘菌・渦鞭毛藻【うずべんもうそう】など、 原生生物は、分類学的には「まとまった系統」ではなく、 『真核生物の初期の特異な多様性の寄せ集め』という性質を持つ。)
太古代(約40〜25億年前)の硫酸還元微生物が利用した 硫酸塩SO42-という電子受容体は、地球誕生直後にはほとんど存在していない。そのため、硫酸がどのように地球表層に供給され、微生物がどのようにそれを利用し始めたのかは、太古代の生物地球化学を理解するうえで非常に重要なテーマとなる。
太古代には、現在のような酸素大気は存在せず、硫酸はほぼすべて「無酸素的な酸化」や「光化学反応」から生まれたと考えられている。
(1) 火山ガス中の硫化水素H2Sの光化学酸化では、太古代の大気に紫外線が大量に降り注ぎ、これが硫黄化合物を酸化した。
その代表的な光化学酸化反応は
H2S + 2H2O + hν ⇒ SO42- +4H+ + 2e-
実際には段階的に進み、 S0(単体硫黄) → SO2 → SO3 → H2SO4(硫酸) という経路をたどる。
中間反応の例 H2S + hν ⇒ S0 + H2
SO2 + H2O ⇒ H2SO3
※酸素は光化学反応で生成した微量のO2や活性酸素が担う。
(2) 海底熱水系での硫黄酸化
熱水中の H2Sが、海水中の酸化剤(Fe3+、活性酸素や微量の酸素)と反応。
H2S + 4Fe3+ + 4H2O ⇒ SO42- + 4Fe2+ + 8H+
これは太古代の海洋で重要な硫酸供給源であった。
(3) 光合成硫黄細菌による硫黄の酸化
酸素発生型光合成より前に存在した「アナオキシック光合成細菌」が、硫化水素を酸化して硫黄や硫酸を生成していた。 H2S + 2hν ⇒ S0 + 2H+ + 2e-
さらに硫黄を酸化する系統も存在した。
S0 + 1.5O2 + H2O ⇒ SO42- + 2H+
太古代の硫酸還元微生物(SRM)は何を電子受容体にしていたのか、現代では硫酸SO42-を使うが、太古代では硫酸が少なかったため、より還元された硫黄化合物を利用していたと考えられている。
(1) 最初期では、硫黄S0やチオ硫酸S2O32-を還元
S0 + H2 ⇒ H2S
S2O32- + 4H2 ⇒ 2H2S + 2H2O
これらは硫酸よりも還元しやすく、酵素系も単純であった。
(2) 硫酸還元の成立(太古代中期の約35〜30億年前)
硫酸が大気・海洋に蓄積し始めると、硫酸還元微生物(SRM)は硫酸を電子受容体として利用するようになった。
代表反応では
● 有機物(例:酢酸)を酸化し、硫酸を還元した。
CH3COO- + SO42- ⇒ 2HCO3- + H2S
● 水素を電子供与体とする場合
4H2 + SO42- + H+ ⇒ H2S + 4H2O
この反応はエネルギー収支が良く、SRMは海底堆積物で大繁栄した。
(3)太古代の硫酸還元が地球に与えた影響
硫酸還元は単なる代謝ではなく、地球環境を大きく変えた。
①ピライト(黄鉄鉱)生成による堆積物の特徴形成
Fe2+ + H2S ⇒ FeS + H+
FeS + S0 ⇒ FeS2
これが太古代の堆積岩に残る「硫黄同位体の非質量依存分別(MIF-S)」の鍵となった。
②海洋の鉄を沈殿させ、バンド鉄鉱床(BIF)形成に寄与
硫化水素が鉄を沈殿させることで、海洋の鉄循環に影響した。
③大気組成の変化に影響
硫酸エアロゾルは気候冷却を引き起こす可能性がある。
目次へ
4)八硫黄(八員環)の構造
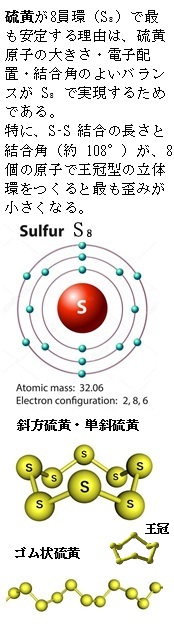 八硫黄Octasulfurの名前の由来は、硫黄原子が 8 個つながった環状分子(S8)であることから「八(はち)+硫黄(いおう)」と呼ばれるようになった。八硫黄は S8(八員環;はちいんかん) の構造をもつ硫黄の代表的な同素体で、8 個の硫黄原子が輪になって繋がっている。 環状構造のS8は、8つの硫黄原子が環状に三次元結合した構造を持ち、各硫黄原子は隣接する2つの硫黄原子と共有結合を形成する。この構造は、電子密度を均等に分布させ、静電反発を減少させることで、分子の安定性を高めている。
八硫黄Octasulfurの名前の由来は、硫黄原子が 8 個つながった環状分子(S8)であることから「八(はち)+硫黄(いおう)」と呼ばれるようになった。八硫黄は S8(八員環;はちいんかん) の構造をもつ硫黄の代表的な同素体で、8 個の硫黄原子が輪になって繋がっている。 環状構造のS8は、8つの硫黄原子が環状に三次元結合した構造を持ち、各硫黄原子は隣接する2つの硫黄原子と共有結合を形成する。この構造は、電子密度を均等に分布させ、静電反発を減少させることで、分子の安定性を高めている。それは、環状構造・結合角・軌道の重なり方が巧みに組み合わさった結果として、『構造の必然性』が極めてよく実現された分子でもある。S8は三次元的にバランスの取れた王冠型Crown-shaped構造をとることで、電子密度が特定の方向に偏らず、環全体に均等に広がる。これが静電反発を減らし、分子の安定性を高めている。
S8の分子は、ほぼ正八角形に近い形をしており、平面ではなく、王冠のように上下にジグザグした構造であるため、各硫黄 S 原子は、ほぼ同じ環境に置かれ、しかも孤立電子対も結合電子対も、互いに最も離れるように配置される。これが、 電子密度が特定の方向に集中させない、エネルギー的に安定した構造となり、原子間の斥力を最小化し、結合を最適化する(原子価殻電子対反発則 valence shell electron pair repulsion rule【VSEPR的効果】)。 しかも、S8では、各硫黄原子が2つの隣接する硫黄原子と共有結合しているため、全体としての強度が高まる。そのため、S8は他の硫黄の多員環分子(例えば、S6やS7)に比べてポテンシャルエネルギーが低く、熱力学的に安定する。 この構造は、自然界で最も一般的に見られる硫黄の形態であり、エネルギー的にも安定する。
(原子は中心にある原子核と、周りを回る電子から構成されている。電子はエネルギーの異なる層(軌道)に分かれて配置され、その中でも最外層の電子を「価電子」と呼ぶ。この最外層が「原子価殻valence shel」にあたる。
原子価殻は、化学結合を形成するために重要な役割を果たす。つまり、化学反応は価電子の移動や共有によって起こるからである。例えば、化学結合は二つの原子の価電子が共有されたり、受け渡されたりすることで成立する。
原子価殻の電子は、エネルギー的に等価な軌道で配置されることが多く、これが「エネルギー的に等価な軌道の組合せ」と言う。つまり、原子価殻内の電子は化学反応において最も活発に関与する部分であり、結合形成に直接的に関与する。)
なぜS8 が安定するのか ⇒ 3 つの核心的理由が存在する。硫黄原子は第3周期元素で、原子半径が長い。そのため S–S 結合は 第2周期元素C–C 結合より長い。C–Cは1.54 Å、S–Sは2.05 Åで約 1.3 倍(1Åは10−10m = 0.1nm )、大きい原子が小さな環(3~6 員環)を作ると、結合角が無理に曲がり、強い歪みが生じる。S8の結合角 108°であれば、 8 員環形成で最も自然に収まる。これは炭素の 理想角109.5°に近く、sp3的な結合角に近い。 109.5° が「理想角」と呼ばれる理由は、4 つの電子対が互いの反発を最小にして最も安定に配置される角度が 109.5°だからである。 しかも硫黄は炭素より柔軟で、8 個の硫黄をジグザグに並べて立体的に折り曲げると、108°が最も歪みのない配置となる。
(sp3混成軌道の結合角度は109.5°で、正四面体の構造をとる。 4つの結合を形成し、その結合は非常に強固で安定しており、飽和結合を形成する。代表的な例としてはメタンCH4が挙げられる。)
7 員環や 9 員環では角度が合わず、ねじれ歪みが増える。 S8の「王冠型」立体構造が歪みを最小化する S8は平面ではなく、王冠のように上下に折れ曲がった立体構造をとる。そのための結合角にも無理が生じない。しかも、S–S 結合のねじれ(torsion)は最小で、原子同士の立体反発が少ない。また、S8 の環は、連続した S–S 結合の鎖でできている。電子が結合軸に沿って広がるため、電子密度が環全体に「なめらかに」分散し、特定の結合に電子は集中していない。結果として静電反発が減少、これは、金属結合ほどではないものの、電子の「ゆるやかな非局在化」と表現できる。自然界で最も多く見られる硫黄が S8であるのは、この安定性のためである。
火山ガスや熱水系で析出する硫黄も、冷却とともにほぼ必ず S8 の結晶(斜方硫黄) になる。これは、地球の表面条件(温度・圧力)で最も安定な硫黄の形が S8だからである。
硫黄は高温では S2 や S3など多様な形をとるが、冷えると エネルギー的に最も低い S8に自然に収束すると言う。硫黄は大きく柔軟な原子であれば、8 員環が最も歪みのない配置で、その王冠型の立体構造が安定性を最大化する。そのため自然界では S8 が標準形態になる。
単体硫黄(元素硫黄)は、黄色い固体として自然界に広く存在し、火山周辺などの自然界から単体としてほぼ純粋な形で得ることのできる元素の 一つ。固形時は淡黄色で無味無臭、点火すると青色の炎を出し、二酸化硫黄SO2の特異臭を発する。その単体の硫黄は、古くよ り火薬 の原料、マッ チの着火燃焼剤、燻煙殺菌や皮膚軟膏の原料として用い られてきた。また、含硫黄有機化合物として、植物や 我々 の体内にも存在する。
硫黄は炭素・水素・酸素・ 窒素に並んで有機化合物に含まれるこ との 多い 元素であ り、人の 体内にも含硫黄ア ミノ 酸がタンパ ク質の 構成成分 として含まれている。
天然に見られる同素体は環状の八硫黄S8で、斜方硫黄・単斜硫黄・ゴム状硫黄という3つの代表的な同素体をもつ非金属元素である。最も安定なのは斜方硫黄で、いずれも主にS8(環状分子)を基本単位としている。
硫黄は、様々な酸化数を取ることが知られている。酸化数が小さい硫化水素H2Sは還元剤として働き、逆に酸化数が大きい三酸化硫黄SO3や硫酸SO4は酸化剤として働く。
目次へ
5)硫酸還元のプロセス
硫酸還元微生物(SRB)は、硫酸H2SO4を還元する過程でATPを生成し、最終的に硫化水素を生成する。このプロセスは「異化型硫酸還元」と呼ばれ、エネルギーを得るために硫酸を大量に還元する。また、これらの微生物は、亜硫酸塩H2SO3やチオ硫酸塩 S2O32-など、他の酸化型無機硫黄化合物も還元することができる。
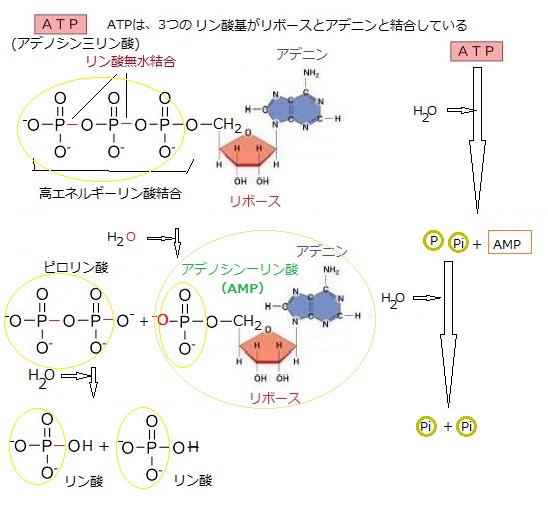 硫酸還元微生物(SRB)が硫酸(H2SO4→ SO42-)を還元する際に ATP を得る反応式は、「硫酸 → APS (アデノシン-5'-ホスホ硫酸)→ 亜硫酸 → 硫化水素」という段階を経て進み、その途中でATPが生成される。
硫酸還元微生物(SRB)が硫酸(H2SO4→ SO42-)を還元する際に ATP を得る反応式は、「硫酸 → APS (アデノシン-5'-ホスホ硫酸)→ 亜硫酸 → 硫化水素」という段階を経て進み、その途中でATPが生成される。硫酸還元微生物がATP 生成する際に硫酸を還元する際に電子供与体(H2や有機物)を利用する。
電子供与体が水素H2の場合が最も基本的で、 この反応の途中で、APS生成のための ATP 消費が起こりるが、 その後の
APS → 亜硫酸SO32-の還元過程で、 基質レベルリン酸化により ATP が生成される。
硫酸還元のエネルギー獲得の鍵は adenosine phosphosulfate(APS)還元反応にあり、
APS + 2e- ⇒ SO32- + AMP
この反応は エネルギー放出反応であり、 基質レベルリン酸化による ATP 生成が結びついていることが示されている。
(ATP の正味収支は微生物種により異なるが、一般に 1 mol (モル)程度の ATP が得られるとされる。1molとは、6.02×1023個(アボガドロ定数)の集団のことを表わす。
分子1molあたりの質量のことを分子量と言う。molが倍になれば、質量なども倍になる。)
硫酸還元微生物(SRB)が使う ATP も、植物が使う ATP も、まったく同じ分子である。 生命圏のあらゆる生物が共有する「普遍的エネルギー通貨」なので、構造も化学的性質も一致している。
ATP(アデノシン三リン酸)は、 アデニンとリボース 、及び 3つのリン酸基 からなる 完全に同一の化学構造を持つ分子で、 細菌・植物・動物・菌類・古細菌など、すべての生命がこれを使っている。 硫酸還元菌が作る ATP も、 植物の光合成で作られる ATP も、 ミトコンドリアで作られる ATP も、 化学式はすべて同じである。 C10H16N5O13P3
違うのは「作り方」と「使い方」だけである。
植物 ⇒ 光合成の光リン酸化 - ミトコンドリアでの酸化的リン酸化 → プロトン勾配を利用して ATP 合成酵素が ATP を作る。
硫酸還元微生物 ⇒ 硫酸 → APS → 亜硫酸 → 硫化物 の還元過程 - 電子伝達系や基質レベルリン酸化で ATP を作る。
硫酸還元微生物のエネルギー源は光ではなく、硫酸還元反応であるが、できあがるATP分子そのものは植物と完全に同じである。
硫酸還元微生物は、土壌や水中の硫酸を減少させ、環境の浄化に寄与する。これにより、植物にとって必要な栄養素を供給し、土壌の肥沃度を高める役割を果たしている。また、これらの微生物は、環境中の有害物質の分解にも関与し、地球の環境を保つ上で非常に重要な役割を果たしながら、自然の循環を助けている。これらの微生物がいなければ、土壌や水中に硫酸が蓄積し、環境が悪化する可能性が高い。硫酸還元微生物は、主に湿地帯や池、川の底などで多く見られ、これらの微生物は水質浄化の研究にも利用されている。
微生物による硫酸還元は、無酸素海底での有機物分解の主要な経路となっている。微生物による硫酸還元による『呼吸』の電子受容体として硫酸塩SO₄²⁻ を使って呼吸する。
有機物 + SO42- → CO2 + H2S(硫化水素)
これは 嫌気呼吸の中で最もエネルギー効率が高い 反応のひとつで、海底の有機物分解の主役であった。
生成された硫化水素H2Sがさらに酸化され、硫黄循環を回す。
硫酸塩 → 硫化物 → 中間硫黄種 → 再び硫酸塩
という複雑な循環が海底で起きていた。
『有機物 + SO42- → CO2 + H2S(硫化水素)』、この反応式そのものはとてもシンプルに見えるが、微生物の内部ではかなり精密な電子の受け渡しが行われている。エネルギーはまさにその電子の流れの中で生まれる。
どこでエネルギーが生まれるのかは、SO42-(硫酸塩)が「電子を受け取る」 というところである。有機物は分解されるときに電子を放出する。SO₄²⁻ はその電子を受け取って還元され、最終的にH2S になる。
この電子が高いエネルギー状態から低いエネルギー状態へ落ちる ときに、
微生物はその落差を利用して ATP(エネルギー通貨)を作る。
これは酸素呼吸と同じ仕組みで、酸素の代わりに硫酸塩が「電子の最終受容体」になっている。
その活用過程は
電子が流れるとき、微生物の細胞膜にあるタンパク質がプロトンH+を膜の外へ汲み出す仕組みを動かす。
• 電子の流れ → プロトンを外へ押し出す
• 膜の内外で 濃度差(電気化学ポテンシャル) が生じる
• その濃度差を使って ATP 合成酵素が ATP を作る
つまり、電子の落差 → プロトン濃度差 → ATP
という流れでエネルギーを獲得している。
反応式の中でエネルギーが生まれるのは、有機物 → SO42-へ電子が渡る電子伝達の過程であり、そのエネルギーは 膜を介した
プロトンポンプ → ATP合成 の過程に使われる。
この循環は、化学合成細菌のエネルギー源や海底の鉱物形成(黄鉄鉱など)となって、海洋の酸化還元構造の維持に深く関わっている。 硫酸塩は大気の酸素と地殻の風化の記録媒体にもなった。
つまり、海の硫酸塩は
大気酸素の増加 → 大陸での硫化鉱物の酸化 → 河川を通じて海へ
という地球規模の変化を反映していた。
海洋大気相互作用でエアロゾル(硫酸塩粒子)を形成し、気候に影響した。
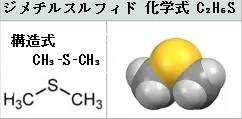
DMS から雲へ至る化学と気候の連鎖
海の表層でプランクトンが放つジメチルスルフィドdimethyl sulfide(DMS)が、大気中で酸化されてMSA(メタンスルホン酸)や 硫酸H2SO4を生み、それらが 硫酸塩エアロゾル となって雲の形成に関わる。この流れは、地球システムの中でも特に美しい「海と空の対話」の一つでもある。海底や海洋の無酸素環境では、硫酸還元菌が硫酸塩を電子受容体として利用し、有機物を分解してエネルギーを得る。 これは海底での有機物分解の主要経路のひとつであり、しかも、海洋炭素循環の根幹を担っていることを示す。
 |
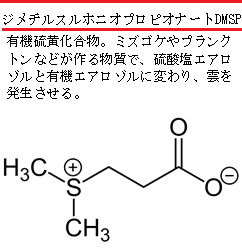 |
| スルホニウム中心(S+)が強い求電子性を持つ。 DMSPの中心には 三置換スルホニウム(R3S+) が存在する。硫黄原子が正電荷を帯びているため、電子不足で非常に求電子的になる。そのため、水 • 塩基 • 求核剤(OH⁻・Cl⁻・アミンなど) によって 容易に攻撃され、分解反応が進む。 スルホニウム塩は一般に「求核攻撃されやすい=不安定」という性質を持つ。 化学的に不安定なため、ジメチルスルフィド (DMS) やメタンチオールに分解し、それぞれがエアロゾルとなり、上空で雲ができやすくなる。 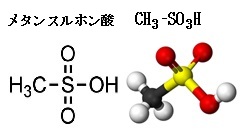 メタンチオール(CH3–SH, S の酸化数 −2)からメタンスルホン酸(CH3–SO3H, S の酸化数 +6)へ至るまでの 酸化段階の連続を、電子の流れが見えるように段階的に示す。 硫黄は −2 → +6 へと、合計 8 電子を失う(酸化される) ことになる。 硫黄は 還元的な −2 から、完全に酸化された +6 へと上がり、 その過程で O が順に付加し、 S–H → S–S → S=O → SO2 → SO3H へと変化していく。 これは、水田・海・湿地などの植物や植物プランクトンが作ることがわかっている。 |
構造の全体像
DMSP は スルホニウム基S+を中心に、
- 二つのメチル基(CH3–)
- プロピオン酸部分(–CH2–CH2–COO-)
両者がが結びついた 内部塩zwitterionの形をとる。
カルボキシル基は海水中でCOO-になり、 スルホニウム基が S+を帯びるため、正負が同居する双性イオンになる。
DMSP の構造が意味するもの
- スルホニウム基(S+) → 強い親水性と安定性をもたらし、浸透圧調整に役立つ。
- プロピオン酸部分(COO-) → 細胞内での溶解性を高め、代謝経路に組み込みやすい。
- 双性イオン構造 → 海水の高塩環境でも安定し、プランクトンの細胞を守る。
DMSP のスルホニウム基が酵素(DMSPリアーゼ)によって切断されると、硫黄を含む部分が ジメチルスルフィドDMSとなって大気へ放出される。
DMSP ⇒ DMS + Acrylate(アクリレート)
DMSP 分解で生じる「アクリレート」とは、アクリル酸の塩またはエステルの総称で、 DMSP の分解で生じるのはアクリル酸の陰イオン(CH2=CH–COO-)のこと。
この反応が、海と大気をつなぐ硫黄循環の核心となる。
DMSP 分解で生じる「アクリレート」は、海洋微生物にとって • 炭素源 • エネルギー源 • 代謝シグナル として利用される、とても反応性の高い分子である。
アクリレートの特徴は、. 二重結合(CH₂=CH–) を持つため反応性が高い。生体内ではすぐに代謝される 。工業的には樹脂・塗料・接着剤の原料として重要 。)
1. 海洋生物が DMS を放出すると
主役は、特に円石藻エミリニア・ハックスレイEmiliania huxleyi などのハプト藻類で、真核微細藻類の一群である。円石藻と呼ばれるこのグループは、美しい円石と呼ばれる炭酸カルシウムの殻というよりは鱗を細胞の周囲に規則的に張り付ける細胞直径5〜50μm程度の植物プランクトンであり、光合成を行う独立栄養生物である。この単細胞藻類には多くの分類群があるが、このバイオマスbiomassを形成するほど大増殖を起こせる分類群は限られている。赤潮生物として有名な渦鞭毛藻(うずべんもうそう)、ライフィド藻、沿岸域の春季に増える珪藻がなどがあげられる。
これらの藻類の特徴として単細胞藻類としては比較的大型(1/100㎜以上)という特徴があるが、円石藻は小型(5/1,000mm以下)で、比較的沖合でも増えることがある。炭酸カルシウムの殻が白く光りをよく反射するため宇宙からでも円石藻の増殖を見つけることができる。このような小さな藻類は、普通は動物プランクトンにすぐ食べられてしまう。円石藻は、食べられない工夫を持っている。その一つがDMSという化学物質だと考えられている。彼らは細胞内で DMSP(ジメチルスルホニオプロピオン酸) を作り、ストレス(光・塩分・捕食など)を受けると DMS(ジメチルスルフィド)に分解して放出する。
DMSが気体として大気に放出されると、雲をつくるもととなる。すなわち、生物が作った化学成分が気候を変えるかもしれない。さらに円石藻の円石は微化石ととなり、海底に堆積し石灰岩のもとにもなる。
2. 大気中で DMS が、酸化されると
太陽光と酸化剤(OHラジカル・NO3ラジカル・O3など)によって次のように変化する。
DMS → DMSO(ジメチルスルホキシド) → MSA(CH4O3S= CH3SO3H)(メタンスルホン酸)
(メタンスルホン酸は、無色・透明の液体、強酸性の有機スルホン酸であり、酸性度は硝酸の17倍、この化合物は、脱水縮合反応の酸触媒や医薬品塩の酸成分として利用される。ただ、非酸化性で、硫酸のような酸化作用は有しないが、吸湿性は高く、濃厚液は水分を吸収しやすい。)
3.海洋生物が作る DMSが酸化されると
海洋生物が放出する DMS(ジメチルスルフィド) が大気中で酸化されると、主要な生成物のひとつとしてメタンスルホン酸Methanesulfonic acid(MSA;CH3SO3H)が大気中で生成される。MSA は揮発性が低く、酸化生成と同時に 硫酸塩エアロソルsulfate aerosol の一部として粒子相に移行する。雲の種とも呼ばれるエアロソルは、気体の中に微小な固体または液体の粒子が浮遊している「気体中の分散系」を指す。 通常0.2μm、つまり雲滴の100分の1の大きさの小さな粒子で、海塩粒子(NaCl) • アンモニア(NH3) • 有機エアロソル などと結びつき、MSA-含有エアロソルを形成する。
MSA を含む硫酸塩エアロソルは 雲凝結核Cloud Condensation Nuclei(CCN) になりやすい性質がある。凝縮核は、大気中の微小な粒子で、水蒸気の液体への遷移には非気体表面を必要とする。凝縮核は、水蒸気が凝縮するための表面 として機能し、凝縮核がなければ、水蒸気は凝縮する表面を持たず、雲の形成はほぼ不可能になる。凝縮核は、雲滴の形成を助けるばかりか、雲の反射率Albedoを高め、地球の放射収支に影響する(冷却方向)。
雨や雪に取り込まれて地表へ沈着するMSAは水溶性が高いため、 湿性沈着(雨・雪) によって海や陸に戻る。
海では再び硫黄循環に入り、陸上では 、光化学反応や微生物分解で硫酸イオンへ変換し、
MSA は環境中で最終的に CH3S3H ⇒ SO42-
のように硫酸イオン(硫酸塩) にまで酸化される。 硫酸塩は、海では栄養塩として利用される。陸では土壌微生物の硫黄代謝に組み込まれる。
海の表層でプランクトンが放つジメチルスルフィドdimethyl sulfide(DMS)が、大気中で酸化されてMSA(メタンスルホン酸)や 硫酸H2SO4を生み、それらが 硫酸塩エアロソル となって雲の形成に関わる。これは気候調節の重要なメカニズムであり、海中の硫酸塩は、単なる溶けたイオンではなく、生物・地球化学・気候の三つをつなぐ『代謝ネットワークの中心物質』として存在感を示す。
大気に出たDMSは酸化され、硫酸塩エアロソルになる。
大気中で DMS は OH ラジカルや NO3ラジカル、O3などによって酸化される。 主な生成物は、硫酸H2SO4やメタンスルホン酸(MSA)、それらが凝結してできる硫酸塩エアロソル これらは 直径数十 nm の微粒子となり、雲の核として働く。
硫酸塩エアロソルは、気候に二つの影響を与える。エアロソル自身が太陽光を拡散し、地表に届くエネルギーを減らす。その間接効果として、雲の性質を変えることで、雲の反射率上昇(トゥーミーTwomey効果)や 雲寿命の延長(Albrecht 効果)などにより総じて 冷却効果 をもたらす。Twomey 効果は、エアロソルによる雲の白さがアルベドを増加させ、地球を冷却方向に働かせる大気科学の重要なメカニズムを指す。 特に人為起源のエアロソルが多い地域では特に顕著で、気候変動評価の不確実性の大きな要因の一つとされている。
雲はエアロソルを核として水滴が形成される。 エアロソルが増えると、雲粒子の数が増え、1つ1つの雲粒子のサイズは小さくなる。雲粒子が小さいほど光をよく散乱する。 雲が白く明るくなる 粒子数が増え、粒径が小さくなると、雲の光学的厚さoptical depthが増し雲のアルベドを上昇させ、より多くの太陽光を宇宙へ反射する。これによる地球の冷却効果(負の放射強制力) を、Twomey 効果では「エアロソル–雲相互作用による第一間接効果」とも呼び、 気候システムに冷却方向の放射強制力をもたらすと理解している。
八ヶ岳山麓の茅野市におけるエアロソル輸送
茅野市は八ヶ岳の山麓〜車山高原に広がる標高差の大きい地域で、 標高 800 m 〜 2600 m の急峻な地形が局地風とエアロソル輸送を強く支配する。茅野市の農業地帯と八ヶ岳・蓼科・車山などの高山帯が密接に相関する日本的な地域構造を持ち、そこで生じるエアロソルは雲形成に特有の影響を与え、気象環境を支配している。
その山岳地形がもたらす特徴 は、上昇流が強い。日中の谷風により、農地や市街地のエアロソルが高標高へ輸送されやすい。その 雲底高度は低い。湿った空気が八ヶ岳にぶつかり、層雲や霧が発生しやすい。
その特有な環境により、微生物や森林由来の揮発性有機化合物Biogenic Volatile Organic Compounds(BVOC)が多く、他方、工業・交通・生活活動から生じる人間の活動によって大気中に放出される揮発性有機化合物anthropogenic Volatile Organic Compounds(anthropogenic VOCs)とが、大気中で酸化され、低揮発性になって粒子化した二次有機エアロソルSecondary Organic Aerosol(SOA)を形成しすい。
SOA ができるまでの流れは、
1. 森林から揮発性有機化合物BVOC が放出される。
2. 大気中でラジカルradicalと呼ばれる非常に反応性の高い種 Hラジカル(H·)、OHラジカル (OH・)、オゾンO3、NO3ラジカル(NO3・ )と反応して酸化生成物ができる。
( Hラジカル(H·) は、電子を1つ失った 裸の水素原子 で、非常に反応性が高い。
大気中では主に H2O + hν ⇒ H・ + OH・ のような光分解で生成される。
有機物(RH)から水素を引き抜く反応が得意で、連鎖反応を開始しやすい。
NO3ラジカル(NO3・);(nitrate radical)
活性は、夜間大気の主要な酸化剤。 光に弱く、昼間はすぐに分解するため 夜間に濃度が上昇する。
VOC(特にテルペンterpeneと速く反応し、二次有機エアロゾル(SOA)生成に寄与する。
代表的な生成反応
NO2 + O3 ⇒ NO3・ + O2
テルペン類は、植物がつくり出す揮発性の炭化水素化合物の大きなグループで、自然界で最も多様な有機化合物の一つ。イソプレン単位(C5H8)を基本ブロックとして重合した天然有機化合物の総称。 植物(特に針葉樹・広葉樹・ハーブ類)が大量に放出する。
O3自体はラジカルではないが、強力な酸化剤。大気化学では、O3が光を受けて、
O3 + hν ⇒ O(1D) + O2
と分解し、ここで生じる励起酸素原子 O(1D) が OHラジカル生成の源 になり、
VOC酸化の起点として極めて重要。)
3. 生成物の揮発性が低下 する。
4. 気体として存在できなくなり、粒子(エアロソル)として凝縮
5. これが SOA になる。SOA の特徴 • 粒径はおよそ 10 nm〜数百 nm • 雲凝結核(CCN)として働きやすい。光を散乱し、冷却効果をもたらし、.霧滴の中でさらに成長する(雲処理)。
茅野市周辺の針葉樹林は、α-ピネン(カラマツやアカマツ針葉樹などの森林の香りの中心)の放出量が非常に多い地域である。 夏の午後、日射が強くなると BVOC の放出が増え、 八ヶ岳の上昇流に乗って高標高へ運ばれる。 そこでオゾンや OH と反応し、 SOA が大量に生成され、霧や雲の核となる。 霧ヶ峰の濃霧が白く厚いのは、 この SOA が霧滴の核として働き、 霧滴が細かく数多くなるためである。 まさに、 森が自らの香りを空へ送り、雲を育んでいる。
硫酸塩は、海の中で『生命・地球・大気』を繋ぐコア機能ハブcore functionality hubのような役割を果たしていた。つまり、海は巨大なスポンジのように酸素を吸い取っていた。
海と空のフィードバックは、.
1. 海が温暖化
2. プランクトン増加 → DMS 増加
3. 硫酸塩エアロゾル増加
4. 雲が増えて厚くなり白さを増す
5. 地表が冷える
海洋生物が呼吸で、温暖化を抑制調節するという視点、もちろん現実はもっと複雑で、地域差や他のエアロソルとの相互作用もあるが、 DMS が気候に影響するという基本構造は確立している。
DMS は「海洋生態系 → 大気化学 → 気候」の橋渡し
海洋生物がDMS を放出→ 大気で酸化され硫酸塩エアロソル→ 雲の形成を助け、反射率を変える → 地球の放射収支に影響→ 気候を調節する。
つまり、DMS は海と空を繋ぐ『気候の分子スイッチ』。
目次へ
