
原生代 25億年前から約5億4,100万年前にあたる地質時代の区分
(地球の胎動と生物の多様な進化)
TOP 車山お知らせ 八ヶ岳火山活動の背景 太陽系の形成
| 目次 | |
| 1)シアノバクテリアと『緑の海』との共進化 | |
| 2)生息環境に合わせた光適応 | |
| 3)太古代のフェリジナス海【緑の海仮説】 | |
| ①太古の海は反応に満ちていた!! | |
| ②太古の海の酸性環境 | |
| ③太古代シアノバクテリアの生態 |
原生代Proterozoic Eonは、地球の歴史における4つの地質学的永劫のうち最も長い時代区分であり、25億年前から約5億4,100万年前にあたる地質時代である。それには冥王代と太古代が先行し、先カンブリア紀の累代の最後の部分である原生代の後にカンブリア紀から始まる顕生代が続く。
原生代の開始の『25億年前』は、明確な地質学的境界がないため、1981年に国際的に扱いやすい便宜的・実務的な「標準値」として25億年が採用された。これは、太古代と原生代の境界に、顕生代の開始のような「世界的に同時に起こった化石の変化」などのような明瞭な地質学的指標が存在しなかったためであった。
名古屋大・京大・東北大などの研究チームでは、原生代の海の光環境を再現し、次のような結論に至っている。当時の地球は酸素がほとんどなく、海には還元状態の二価鉄(Fe2+)が大量に溶け込んでいた。やがてシアノバクテリアによる光合成で生まれた酸素が鉄を酸化し、微細な酸化鉄(FeO・Fe2O3)が海中に漂った。この酸化鉄の粒子は、紫外線や青い光を強く吸収する。また、水そのものは赤い光を吸収する性質がある。残るのは緑、その結果、海は緑色の光を吸収せずに反射するため、緑色に輝いていたと見ている。
最新の研究では、シアノバクテリアは、太古の海が緑色の光で満たされていた環境で、その光を効率よく吸収する光アンテナ(フィコビリンphycobilin)を進化させ、繁栄していたことを示す。
フィコビリンは、シアノバクテリアが持つ光捕集色素で、フィコビリソームphycobilisomeというアンテナ複合体の中に組み込まれている。進化させたフィコビリンにより、光エネルギーの吸収範囲を広げた。フィコビリンは 赤・橙・黄・緑(520〜630 nm)の光を効率よく吸収する。これらの波長はクロロフィルaが苦手とする領域なので、シアノバクテリアはより広い光環境で光合成できるようになった。
(クロロフィルaは、可視光のうち青色域の吸収ピークは430nm前後 と 赤色域の吸収ピークは、約662nm前後の光を強く吸収する。クロロフィルaは、青と赤の光を強く吸収し、緑の光をほとんど吸収しないため、植物は緑色に見える。)
 フィコビリンはフィコビリプロテインphycobili proteinと言うタンパク質と結合し、光捕集アンテナphycobilisomeを形成する。ここで吸収した光エネルギーは、効率よく光化学反応中心((光化学系II;photosystem II【PSII】など)へ転送される。
フィコビリンはフィコビリプロテインphycobili proteinと言うタンパク質と結合し、光捕集アンテナphycobilisomeを形成する。ここで吸収した光エネルギーは、効率よく光化学反応中心((光化学系II;photosystem II【PSII】など)へ転送される。PSIIは光合成の中で、光をエネルギーに変換する最初のステップで、水を酸化して電子を取り出す能力があり
水 → 電子 + プロトン (H+) + 酸素(O2)
ここで生じる酸素が、地球の大気を満たすO2の源であり、励起された電子はプラストキノンplastoquinone(PQ)へ渡され、失われた電子は水の分解で補われる。プラストキノンは、植物や藻類の光合成で使われる重要な電子運搬体で、特にPSIIから電子を受け取り、次のシトクロムb6f複合体へ運ぶ役割を担っている。また酸素を生み出す唯一の装置であり、ATPとNADPH生成の起点となる電子を供給する中心的存在と言える。
シトクロムb6fは、PSIIでプラストキノン(PQ)が 2つの電子と 2つのプロトン(H+)を受け取って還元されたプラストキノールplastoquinol(PQH2)から電子を受け取り、PSIへ渡す中継点であり、これにより、光合成の二つの光化学系が一つの流れとして結び付く。
プラストキノンは、葉緑体やシアノバクテリアが持つ主要キノンで、この光合成の電子伝達に関わる炭化水素系の芳香族環は、化学的に非常に頑丈で、繰り返しの酸化還元に耐えられる。また、芳香族環は「疎水性」で膜中を移動しやすい。生体内のキノン(ユビキノン、プラストキノン)は、電子伝達系でミトコンドリア内膜やチラコイド膜の中を横方向に移動する。この移動には 疎水性の炭化水素環が重要で、そのため膜の中を自由に動ける。
つまり、炭化水素系の芳香族環は、電子伝達のための化学的安定性が高く、また膜中移動のための物理的特性の両方を満たす、非常に合理的な構造になっている。
酸化型プラストキノン(PQ)→セミキノン(キノン類の中間の酸化段階にある遊離基)→還元型プラストキノール(PQH2)と変化しながら電子とプロトンH+を運ぶ。特に PQ-9(プラストキノン9)が主要成分で、PSIIの2つのプラストキノン電子受容体QA(一次電子受容体)・QB(二次電子受容体)部位で電子受容体として働く。
QA(一次電子受容体)は、PSII の最初の安定な電子受容体で、化学的本体は プラストキノン(PQ)であり、電子だけを受け取るタイプ(1電子酸化還元)で、D2タンパク質に結合している。
D2タンパク質は、光エネルギーを効率的に捕集するための補助色素と結合し、光合成反応において重要な役割を果たしている。D2タンパク質は、光化学系Ⅱの二次電子供与体として機能し、光化学系Ⅱの酸化還元反応に関与する。D2タンパク質のアミノ酸配列はD1タンパク質と相同性が高く、構造的にも機能的にもD1タンパク質との類似性がきわめて高い。
(光化学系Ⅱの機能が低下すると、光合成効率が著しく低下し、植物の成長に深刻な影響を及ぼす可能性がある。環境ストレスによる光化学系Ⅱの損傷は、植物の生存にとって重大な脅威となっている。)
QB(二次電子受容体)は、QA の次に電子を受け取る 第二のキノン受容体で、2つの電子を順番に受け取り、PQH2(プラストキノール)として膜へ放出し、D1タンパク質の上にある QB 結合部位に結合させる(除草剤の標的として有名)。QA は電子を一時的に保持するだけだが、QB は電子を2つ受け取り、プロトンも2つ取り込んで PQH2 となり膜中へ移動する。
つまり、QA は、固定された電子受容体で動けないが、QBは、電子を受け取って膜中へ出ていく可動型受容体という役割を分担している。
QAは、1つの光化学反応で電子は1つしか出ない。しかし PQH2を作るには電子2つ+プロトン2つが必要、そのため2つのQA から電子を一つずつ受け取り、QB がその2つの電子を集めて PQH2にする。という二段階構造が必要になる。
また、PSIIから出た電子は、PSIへと流れ、最終的に NADP+→ NADPH の還元に使われる。PSII で生まれた電子は プラストキノン(PQ) に渡される。PQ は電子とプロトンH+を受け取り PQH2となり、葉緑体の膜内を移動して、 シトクロムb6f複合体に電子を渡す。
シトクロム b6f複合体は、葉緑体のチラコイド膜に埋め込まれている膜タンパク質複合体(植物の葉緑体 • シアノバクテリア • 緑藻 など、これらの生物の チラコイド膜thylakoid membraneに存在することが明確に示されている。)で、光合成電子伝達系では、PSIIとPSIを繋ぐ中心的な電子輸送複合体と言える。プラストキノール(PQH2)を酸化し、プラストシアニン(PC)を還元する過程で プロトンをチラコイド膜内腔へ輸送し、ATP 合成に必要なプロトン勾配を形成 する重要な役割を担っている。
この過程では、葉緑体のチラコイド膜で囲まれた内腔のルーメンlumenは、光化学系の水分解や電子伝達、そしてATP合成のプロトン勾配形成など重要な役割を担っている。葉緑体のストロマ側からルーメン側へ H+が汲み上げられ、プロトン勾配が形成される。ここは水由来のH+.がエネルギーへと変換される段階に至る。
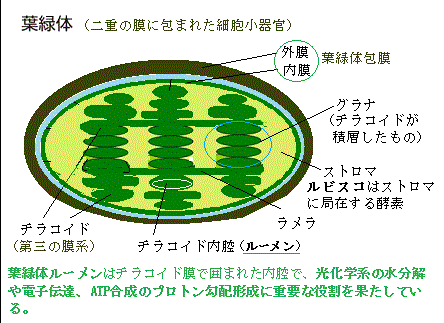 |
| チラコイドルーメンthylakoid lumenでは、ルーメンに輸送される多くのタンパク質を、流入後に「プロセシングprocessingを行う。 ここでいう「プロセシング」とは、タンパク質がルーメンに到達した後に受ける切断と成熟化の処置を言う。 葉緑体に輸送されるタンパク質の多くは、核で作られた後に葉緑体へ運ばれる。 その際、輸送のためのシグナル配列(ターゲティングペプチド)が付いている。 そのため、ルーメンに到達した後、そのシグナル配列を切断し、正しい構造に折りたたみ直すため、ルーメン内でのプロセシングが必須になる。 また、ジスルフィド結合disulfide bondは、2つのチオール基(-SH)が酸化反応を通じて結合し、形成される共有結合で、この結合は、構造式R-S-S-R'で表され、この2つの硫黄原子による共有結合構造をSS結合やジスルフィド架橋と呼び。 この過程は、細胞内での複雑な生化学的反応の一部として行われ、特にタンパク質の立体構造の安定性が高まる。そのジスルフィド結合は、タンパク質がその機能を果たすために適切に折りたたまれることを助ける重要な役割を担う。 特に、システインというアミノ酸が含まれるタンパク質において、ジスルフィド結合はその三次構造の形成に寄与し、タンパク質の安定性を高める。このため、多くの生物学的過程において不可欠な存在であり、特に酵素の活性や細胞間の信号伝達に重要となる。 これらの処理を行うために、ルーメンには以下のような酵素が存在する。 プロテアーゼ(タンパク質切断酵素) → タンパク質のシグナル配列を切断し成熟化させる。 プロリルシストランスイソメラーゼ → タンパク質の立体構造形成を助ける。 ペルオキシダーゼ、ポリフェノールオキシダーゼ → 酸化反応に関与。 ビオラキサンチンデエポキシダーゼ → キサントフィルサイクルに関与(光防御)。 チラコイドルーメンでのプロセシングとは、ルーメンに輸送されたタンパク質が 成熟化(切断・構造調整・修飾)される過程のことを言う。 これを行うための酵素がルーメン内に存在する。光合成に必要なタンパク質が正しく働くためには、不可欠なステップとなる。 |
光合成の電子伝達反応に共役して、H+がチラコイドルーメンに輸送されるため、明条件ではルーメンはpH5くらいまで酸性化する。このルーメンのpH変化は、いくつかのタンパク質のプロトン化や、キサントフィルサイクル関連酵素の活性変化を引き起こし、光合成が光環境に応じて調節されるメカニズムの一端を担っている。
ルーメンに輸送されるタンパク質の多くは輸送後プロセシングを受け、そのためのプロテアーゼが存在する。ここでいう「プロセシング」とは、 タンパク質がルーメンに到達した後に受ける『切断・成熟化』のことで、具体的にはは前駆体タンパク質pre-proteinからシグナル配列を切断する タンパク質を正しい立体構造に整える。.また、 ジスルフィド結合の異性化など、機能発現に必要な修飾を行う これらの処理を行う。.このため.ルーメンには多種の酵素が存在する。
シトクロムb6f で電子は段階的にエネルギーを失いながら 銅タンパク質プラストシアニン(PC)に渡される。PC はチラコイド膜表面を滑るように移動し、PSI へ電子を届ける。.
PSI(光化学系I)で再び光励起される。PSI の反応中心 P700 が光を吸収し励起(P700*)する。 P700* は電子を失うと、PC から電子を受け取って補う。P700* から放出された高エネルギー電子は、還元型フェレドキシン(Fdred)に渡される。
フェレドキシン(Fdred) → FNR → NADP+還元
フェレドキシン(Fdred)は、電子を『フェレドキシン-NADP+レダクターゼ(還元酵素FNR)』に渡す。FNR は、 「光合成電子伝達系の最終ステップで、電子を NADP+に渡して NADPH を作る酵素」 であり、 生命の還元代謝を支える中心的な電子変換装置である。シアノバクテリアや植物葉緑体のチラコイド膜および根の色素体plastidに存在し、還元型フェレドキシンによるNADP+の還元によりNADPHを生成するのに必要な可溶性酵素であり、次の反応を可逆的に触媒する。
FNR は電子とプロトン(H+)を使って 、
2分子の還元型フェレドキシン(Fdred) + NADP+ + H+ ⇔ 2分子の酸化型フェレドキシン(2Fdox) + NADPH
NADPH はカルビン回路で CO2 を還元し、糖を作るための『還元力の通貨』として働く。
水の分解で生じたプロトンH+は、ストロマ側からルーメン側へ 汲み上げられた後に、ATP合成酵素がATPを作るためのプロトン勾配を形成する。
目次へ
• 浅い場所にいる種は、青・緑、黄〜赤光を吸収するフィコビリンを多く持つ。
• 深い場所にいる種は緑光を吸収するフィコエリトリンを増やす傾向がある。
光合成色素は、光合成をするときに光を受容するアンテナの役割をする。植物(コケ植物・シダ植物・裸子植物・被子植物)は、クロロフィルaとクロロフィルbをもち、緑藻類と同じ種類の光合成色素をもっている。このため、緑藻類・紅藻類・褐藻類・ケイ藻類などの藻類がある中で、陸上植物は特に緑藻類と近縁であると考えられる。
ただ、現代の分類学では「藻類は植物ではない」 。現在は、進化の系統(どの祖先から進化したか)を重視するため、藻類は植物とは別扱いになる。つまり、藻類は多系統で共通の祖先は一つではない。シアノバクテリアのように細菌に近い藻類もいる。緑藻・紅藻・褐藻など、進化的にバラバラのグループが含まれる。つまり「藻類」という言葉は、光合成をする多様な生物の寄せ集めにすぎない。シアノバクテリアのように細菌に近い藻類もいる。 緑藻・紅藻・褐藻などは、進化的にもそれぞれがバラバラのグループであり、つまり「藻類」という言葉は、光合成をする多様な生物の集合体を指す。
現代の分類では、陸上植物(コケ植物・シダ植物・種子植物)を「植物」とする考え方が一般的である。 この定義では、藻類(海藻など)は、 植物ではない という扱いになる。ただ、緑藻green algaeを植物に含める場合もある。緑藻の中には、陸上植物により近いシャジクモ類などのグループ(水草のような姿をした大型の藻類、極めて複雑な生殖器官をもつ。DNAに基づく分子系統解析からも、に陸上植物に最も近縁な生物群の1つであることが示唆されている。多くは淡水止水域に生育し、特に湖沼では比較的深い水深まで分布している。水質汚濁などによって絶滅危惧種となっているものが多い。)があり、 これらは緑藻植物門から除外され、陸上植物と同じ「ストレプト植物Streptophyta」に分類されている。 これは、 緑藻の中に陸上植物の祖先に極めて近い系統が存在する ことを示している。
ストレプト(strepto-, strepsis)は、ギリシア語で「らせん」を意味し、この系統の多くの生物(接合藻を除く)で精子がらせん状にねじれていることに由来する。陸上植物の祖先はストレプト植物の淡水藻類から進化した。陸上植物に特有と思われていた遺伝子の多くが、実はストレプト植物の藻類にも存在する。ストレプト植物は、地球史・進化・植物の繋がりが凝縮された系統群であった。こうした研究により、植物がどのようにして陸上へ進出し、今日の多様性を生み出したかを解き明かす。
(最も古い生命活動の痕跡として有名なのが ストロマトライトstromatoliteで、シアノバクテリアが堆積物を取り込みながら作る層状構造で、20億年前のものは確実にシアノバクテリア由来とされる。さらに35億年前のストロマトライトもあるが、生物起源か無機起源か議論が続いている。つまり、20億年前以降は確実、35億年前は議論中という状況。)
| 光合成の補助色素とその機能 | |||
| 色素名 | 外観の色 | 主な吸収光 | 主な生物 |
| フィコシアニン | 青 | オレンジ〜 赤(620 nm) |
シアノバクテリア |
| アロフィコシアニン | 青緑 | 赤(650 nm) | シアノバクテリア |
| フィコエリスリン | 赤〜橙赤 | 緑光 | 紅藻・ シアノバクテリア |
| フィコビリン (発色団) |
赤・青緑 黄色など |
種類による | シアノバクテリア 紅藻・クリプト藻 |
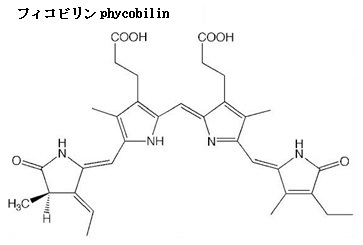 フィコビリンは、藻類に含まれる水溶性の色素タンパク質で、光合成の補助色素として重要な役割を果たす。 フィコビリン色素と結合するタンパク質『フィコビリプロテイン』は、シアノバクテリアや特定の藻類にあって、光エネルギーを捕捉し、光合成の主要素クロロフィルへと伝達する。 このフィコビリプロテインは、タンパク質同士が共有結合し一つの分子となるフィコビリンの複合体を形成し、発色団として機能する。 これらのタンパク質は、順次結合を重ね発色団の数を増加させ、タンパク質の外側表面に付加することが構造解析から裏づけられている。 |
|||
シアノバクテリアや藻類では、フィコシアニンはフィコビリソーム(光捕集複合体)の一部として働く。620 nm 付近の光を吸収し、650 nm の光では、「余剰エネルギーの漏れ」として蛍光を放つ。結果、必要なエネルギーだけを光合成反応中心へ効率的に伝達する。その蛍光は、光捕集の効率を測る指標として利用されている。
フィコシアニンはスピルリナの中に含まれる『青い宝石のような色素タンパク質』で、スピルリナはシアノバクテリアの一種で、淡水・汽水域に生息する地球最古級の生命体と言われている。タンパク質・ビタミン・ミネラル・抗酸化物質が非常に豊富で、「スーパーフード」と呼ばれる理由は、この総合的な栄養価の高さにある。
アロフィコシアニンallophycocyaninは、シアノバクテリアの光合成アンテナ『フィコビリソーム』のコア部分を構成する主要色素タンパク質で、フィコシアニンよりやや緑がかる青緑色、主に 赤色光(約650 nm)を吸収する。フィコビリプロテイン(光捕集色素タンパク質)の一種、発色団フィコビリンを持つ。フィコビリソームの中心部で、最終的に光エネルギーを光化学系 II に渡す。
フィコビリンphycobilinは、シアノバクテリア・紅藻・クリプト藻などが持つ水溶性の光合成補助色素で、タンパク質と結合してフィコビリプロテインを形成する。これらは光捕集アンテナ複合体フィコビリソームを構成し、クロロフィルが吸収しにくい波長の光を効率よく吸収する。外観の色は、赤・青緑・黄など。主な吸収光は、生物それぞれの種類による。
フィコエリスリンphycoerythrinは、緑光の光合成に関与する赤色のフィコビリタンパク質で、主に紅藻やシアノバクテリアに存在する。外観の色は、鮮やかな赤色から橙赤だが、緑〜黄緑光をよく吸収する。
紅藻やシアノバクテリアのフィコビリタンパク質の分子内には光合成でクロロフィルに光エネルギーを渡す補助色素C-フィコエリスリンやR-フィコエリスリンなど複数のタイプが含まれている。吸収極大は565 nm、蛍光極大は577 nm。天然の色素として食品や化粧品に使用されるほか、免疫測定のための試薬としても利用されるなど、諸研究においてもモデルタンパク質として利用される。
フィコエリスリンは、光合成においてクロロフィルに光を伝える役割を果たし、特に緑色の光を吸収しにくい植物にとって重要である。フィコエリスリンは、光合成において重要な役割を果たし、クロロフィルの酸素生成効率を高めることが知られている。つまり、フィコエリスリンは、クロロフィルが吸収できない波長の光を補完し、効率的にエネルギーを渡すことで酸素発生(O2 evolution)を強化する。
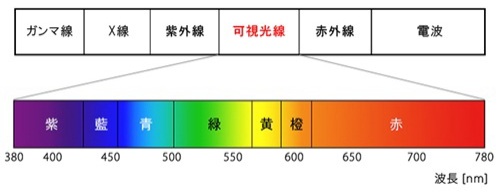 クロロフィル a は、 青色域と赤色域で強い吸収ピークを持つ。青色では、 約 430 nm 前後が 高エネルギー光で、励起効率が高い。赤色では、約 662〜668
nm(溶液中で 662 nm、蛍光ピークは 668 nm) が、 光合成の反応中心、特に PSIIで重要な役割を果たす。
クロロフィル a は、 青色域と赤色域で強い吸収ピークを持つ。青色では、 約 430 nm 前後が 高エネルギー光で、励起効率が高い。赤色では、約 662〜668
nm(溶液中で 662 nm、蛍光ピークは 668 nm) が、 光合成の反応中心、特に PSIIで重要な役割を果たす。緑〜青緑光への反応では、 一般に「クロロフィルは緑を吸収しない」と言われているが、これは 『吸収が弱い』のであって、完全に吸収しないわけではない。 緑〜青緑光(約 500〜550 nm) ではクロロフィル a の吸収は弱いが、葉全体としては 光合成に利用される。特に、緑光は葉の内部まで深く透過し、深部のクロロフィルを励起できる。そのため、光合成の量子収率は赤・青より低いが、葉の厚い植物では意外と重要な光になる。
フィコエリスリンはこの『光の谷』の光量子を強く吸収する。フィコエリスリンの発色団のフィコエリスロビリンphycoerythrobilin(PEB)による赤色吸収するが、一部の種では、最大吸収範囲が約495 nmに及ぶフィコウロビリンphycourobilin(PUB)により青緑光も吸収して利用可能な光エネルギーの総量が増やす。
フィコエリスリンが酸素生成を高める理由は、クロロフィルが吸収できない波長の光も吸収し、フィコビリソームphycobilisomeで高効率にエネルギーを伝達すると、PSII の励起が高まり.水分解(O2 発生)が促進され、発色団フィコエリスロビリン(PEB)の高い量子収率も寄与して、光環境に応じた構造変化も加担し、その効率を最適化される過程をたどることによる。
シアノバクテリアや紅藻の光合成を理解するうえで、フィコビリソームは『色の扇の要』のような美しい構造を持つ、巧妙なエネルギー伝達機構を持つ『巨大な超分子アンテナ複合体』として存在する。フィコビリソームは、チラコイド膜の細胞質側(ストロマ側)に規則的に半円盤状(扇形)に並ぶ巨大複合体で、その扇の中心(要;かなめ)が膜に接している。
シアノバクテリア・紅藻・グロコシアニン藻(灰色藻;かいしょくそう)の主要アンテナ複合体で、光化学系 II(PSII)へのエネルギー供給が主な役割で、一部では 光化学系 I(PSI)にもエネルギーを渡すという説もある
浅い場所では光が強く、青光が強く散乱し、 黄〜赤光が比較的安定して届くため、これを吸収できるフィコビリンが有利になる。 特に紅藻は、 緑色の光を吸収するフィコエリスリンphycoerythrin(吸収:緑光) やフィコウロビリン(吸収:青緑光) を多く持ち、浅場の光環境に最適化されている。また、紅藻はフィコエリスリン(緑光)とフィコシアニンphycocyanin(橙~赤)の光合成補助色素を豊富に持ち、浅海〜中層の強い光環境でも効率よく光を吸収できるため、浅い海に多く生息する。多くの紅藻は緑光.を吸収するフィコエリスリンを多くもつため、その名の通り葉緑体は紅色を呈するが、フィコビリンタンパク質の組成や他の色素との量比によって青緑色・オリーブ色・紫色などの色調を呈するものもいる。
紅藻には フィコエリスリン という緑色の光合成補助色素が豊富に含まれている。この色素が 青〜緑の波長の光を強く吸収し、赤光を反射 するため、紅藻全体が赤く見える。
海水は赤い光を吸収するから、深くなるほど青や緑の光だけが届きやすい環境になる。フィコエリスリンはこの青緑光を効率よく吸収できるため、紅藻は比較的深い海域でも光合成が可能となり生息できる。
シアノバクテリアは多様な光環境に適応できる。緑光を吸収するフィコビリンの量や種類は、窒素濃度などの環境条件で変化することが報告されている。これは光合成効率や代謝の調整に関わると考えられている。フィコビリン色素は、シアノバクテリアの進化の過程で、より「光の届き方が限られた世界で生き抜くための、柔軟で強力な光捕集システム」を確立し適応した。
アノバクテリアが 「光環境」や「窒素濃度」などの環境条件に応じて、フィコビリン(フィコエリスリン・フィコシアニンなど)の量や種類を変化させる仕組みは、実はとてもダイナミックで高度である。シアノバクテリアは、周囲の光の色に応じて フィコビリンの種類を切り替えることができる。 これを chromatic acclimation(色順応) と呼ぶ。
緑光が強い環境では、フィコエリスリン(PE)や フィコウロビリンphycourobilin(PUB)を増やす。緑光〜青緑光を効率的に吸収するためフィコビリソームのロッド構造が長くする。赤光が強い環境では、フィコシアニン(PC)を増やす。赤光吸収を最適化するため ロッド構造が短くする つまり、光の色に応じて「光捕集アンテナの色と形」を作り替える。
窒素が豊富なときは、フィコビリソーム(PBS)を大きくし、フィコビリン量を増やし、光捕集能力を最大化させ成長速度を上げる (窒素はフィコビリンタンパク質の主要構成要素)。窒素が不足したときは、PBS を分解して窒素を回収する。フィコビリソーム分解エフェクターPhycobilisome Breakdown Effector(NblD )などの分解因子が働くことが報告されている。 分解されたアミノ酸は細胞の維持に再利用される。光捕集能力は低下するが、窒素枯渇環境でも生存できる。窒素欠乏時に PBS が分解されることが明確に示されている。
具体的には、光が弱い+窒素が豊富であれば、フィコビリソーム(PBS)を増やし、フィコエリスリンPE や フィコシアニンPC を多く合成する。光が強い+窒素が不足であれば、 PBS を縮小し、光ストレスと窒素不足の両方に対応して、光の色が変化 → PE ↔ PC の比率を調整する(色順応) 。このように、シアノバクテリアは 光の量・光の色・窒素濃度 という複数の環境要因を統合して、PBS の構造を最適化する。
合成側でも、 光センサー(RcaE など)が光の色を検知し、 PE や PC の遺伝子群(cpeA/B、cpcA/B など)の発現を調整 し、発色団(フィコエリスロビリンPEB、フィコウロビリンPUB)の合成酵素も調整する。分解側でも、窒素欠乏時、 NblA、NblD などの PBS 分解因子が誘導される。 PBS が段階的に分解され、アミノ酸として再利用され、これにより窒素バランスを維持する。
湖沼・海洋・温泉・土壌など、光環境が大きく異なる。深度によって光の色が変わる(青緑光が優勢)。窒素濃度も場所によって大きく変動する。そのため、シアノバクテリアは 光捕集アンテナ(PBS)を可塑的に作り替える能力 を進化させたと考えられている。
目次へ
3)太古代のフェリジナス海【緑の海仮説】
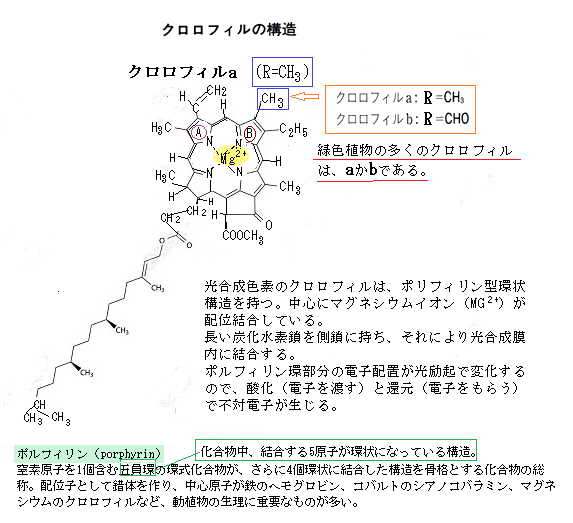 |
| 光合成の前半部で起こる「チラコイド反応」を司るいくつかの分子が、チラコイドの膜上に埋め込まれている。その中の2つが、光のエネルギーを受け取る「光化学系(PS)」というタンパク質複合体だ。 「光化学系(PS)」には「光化学系Ⅰ」と「光化学系Ⅱ」の2つがあり、反応の順番は「光化学系Ⅱ」が先に作用して、その後に「光化学系Ⅰ」が作動する。 光エネルギーの反応を別の視点からみると、「アンテナ複合体LHC」に結合している様々な光合成色素が、幅広い波長の光を集め、その光のエネルギーを、光合成反応にスイッチを入れる「反応中心複合体」に受け渡しをする。その「反応中心複合体」の主要部分が「反応中心」と呼ばれる「クロロフィルa」なのだ。最終的に「クロロフィルa」が光のエネルギーを受け取る。 陸上植物では、「クロロフィルa(青緑)」と「クロロフィルb(黄緑)」の割合が約3:1と知られている そのため「クロロフィルa」は「主色素」と呼ばれ、その他は「補助色素」と呼ばれることがある。 |
太古代後期の約30〜25億年前の海では、海水中に溶けた大量の二価鉄Fe2+が、シアノバクテリアの光合成で生まれた酸素によって酸化され、その酸化鉄(FeOやFe2O3など)粒子が 紫外線〜青色光を強く吸収 したため水中には緑の光だけが豊富に残った。つまり、シアノバクテリア自身が放った酸素が、海の光環境を緑色に変えた。
シアノバクテリアは、緑の光を吸収する『フィコビリン色素』を持つ光アンテナを早期に適応進化させ、その光アンテナが 緑の光環境で特に有利に働いた。その結果、シアノバクテリアは太古の海で繁栄し、その後に 葉緑体の起源 となる系統へつながった。これが『緑の海仮説Green Ocean Hypothesis』と呼ばれている。
『緑の海仮説』とは、名古屋大学・東北大学などの研究チームが2025年に提唱した仮説で、太古代(約30〜25億年前)の海は青ではなく『緑色』に満ちていたと提唱した。その根拠は、シアノバクテリアが放出した酸素が、海に溶けていた二価鉄Fe2+を酸化し、その生成物が紫〜青の光を吸収してしまったためと説く。その結果、水中には緑色の光だけが豊富に残る「グリーンライト・ウィンドウgreen light window」が形成された、と考える。
太古代の海は、鉄に満ちていた。.大気はほぼ無酸素で現代とはまったく異なる化学環境であった。フェリジナス海ferruginous oceanである太古の海で起きていた Fe2+→ Fe3+(鉄水酸化物) の酸化反応は、地球史の根幹をなす美しい化学プロセスであった。「太古代のフェリジナス海」は、酸素がほとんど存在しない環境で、海水中に大量の Fe2+(二価鉄=還元鉄)が溶けていた状態の海を指す。また、陸地の侵食が速く、鉄が大量に海へ流入し、海水は酸性寄りに海全体に二価鉄 Fe2+が溶けていた。
(フェリジナス海ferruginous oceanの語源は、ferrum(鉄)+ -genous(〜に富む)から来ている。太古代〜原生代前半の大気は、酸素が極めて少なく、海も無酸素anoxicであった。ギリシャ語の「an-」(無、欠乏)と「oxy-」(酸素)から派生している。酸素がないため、鉄は酸化されず、Fe2+のまま海水に大量に溶け込むことができた。このフェリジナスな状態が、地球史の大部分で支配的であった。 特に、太古代(40〜25億年前) • 原生代前半(25〜18億年前) の海は、ほぼ全てフェリジナスであった。)
フェリジナス海で Fe2+が酸化されて Fe3+(酸化鉄)になるとき、反応式に H+が出てくるが、その H+ はどこから来たのか」という問題が.生じる。シアノバクテリアが放出した O2 によって、溶存鉄(Fe2+)はまず酸化される。微細粒子Fe3+が海中に漂う。実際に太古の海で起きていたと考えられる 代表的な化学反応式 を、段階的に示すと
4Fe2+ + O2 + 4H+⇒ 4Fe3++2H2O
これは「二価鉄Fe2+ → 三価鉄Fe3+」への純粋な酸化反応である。ここでの プロトンH+は「反応式の都合」であり、外部から特別に供給される必要はない。これは「酸性条件下での酸化反応」を表しているだけで、 太古代の海は微細粒子Fe3+が海中に漂う。
結論から言うと、その H+は「フロンHF」のような特殊な供給源ではなく、太古代の海そのものが本来もっていた酸性度と、火山ガス・二酸化炭素・硫黄化合物などによって供給されていた。
実体は 水和したプロトン(H3O+)
また、水を吸収して光合成を始めたシアノバクテリアが酸素を放出すると
2H2O ⇒ 4H+ + 4e- + O2
この反応で もプロトンH+が生じる。
シアノバクテリアの光合成そのものも がプロトンH+の供給源であった。
太古代の海は、CO2による酸性 • 火山ガスによる酸性 • 光合成による H+生成 によって、常に十分なプロトン H+を含んでいた。つまり、現代の海よりもH+が豊富で、はるかに酸性であった。
ただ、化学では H+という表記はよく使われるが、「H+という名前の物質」が存在するわけではない。
水素の原子は、1つの陽子と1つの電子により構成されている。一般名のプロトン(proton)H+は、水素原子が唯一の電子を失った状態である。 H+は電子がなく、陽子(proton)1個だけの存在であれば、H+は 「プロトン」 と呼ばれる。
実際の水の中では、裸の H+は存在できない。 水分子にすぐ取り囲まれて、次の形になる。
H++ + H2O ⇒ H3O+ (オキソニウムイオンoxonium ion)
その実体は、 CO2や火山ガスによって酸性化された海水中の水和プロトン(H3O+)を意味する。水(H2O)は代表的な極性分子で、他の多くの極性分子と水素結合を作りやすく、水和反応は水の分子が反応物に近づき、HとOHが新しい結合を作る反応のことを指す。言い換えると水が化学反応に参加して物質の性質を変える現象を示す。また水分子相互間の水素結合形成は、通常、よりいろいろな大きさや形状のクラスターclusterを形成する。
フェリジナス海ferruginous oceanで Fe2+が酸化されて Fe3+(酸化鉄)になるとき、反応式に H+が出てくるが、その H+は太古代の海そのものが本来もっていた酸性度に加え、火山ガス・二酸化炭素・硫黄化合物などによって補給が途絶えることはなかった。
三価鉄(Fe3+)はすぐに水酸化物として沈殿する。
Fe3+は水中では非常に不安定で、すぐに水と反応して 鉄(III)水酸化物(いわゆる赤錆の前駆体)になる。
Fe3+ + 3H2O ⇒ Fe(OH)3 + 3H+
この沈殿物の鉄(III)水酸化物Fe(OH)3が、太古の海底に積もって 縞状鉄鉱層Banded Iron Formation(BIF) を形成していく。現在、工業的に使われる鉄鉱石の大半がこの縞状鉄鉱床から採掘されている。
上の2つをまとめると、太古の海で起きていた代表的な総合反応は次のように書ける。
4Fe2+ + O2 + 10H2O ⇒ 4Fe(OH)3 + 8H+
つまり、O2 が Fe2+を酸化する。 Fe(OH)3が沈殿するとH+が生成され、海がさらに酸性寄りになる。という、地球化学的なフィードバックが働く。これは「二価鉄Fe2+ → 三価鉄Fe3+」への純粋な酸化反応であり、しかも、これらが 紫外線〜青色光を強く吸収する。
②太古の海の酸性環境
水自体は赤色光を吸収する。水はもともと赤色光を吸収しやすい性質を持つ。結果、緑色光だけが残る。青は鉄粒子に吸収され、赤は水に吸収される。
残ったのは緑色光、これが太古の海を「緑色」に染めたと考えられている。
シアノバクテリアは、クロロフィルだけでなく、フィコビリン(フィコビリソーム) という色素タンパク質を持ち、緑色光を効率よく吸収する光アンテナを保持した。つまり、緑色光が豊富な海で生き残るためにフィコビリンを進化させた。環境が光のスペクトルを変え、その光環境が生物の光合成装置を進化させ適応した。緑の海で繁栄したシアノバクテリアは、やがて地球の酸素濃度を上昇させる 大酸化イベントGreat Oxidation Event(GOE)を引き起こす。
植物は、緑色の光をほとんど吸収せず、主に反射・透過しているため緑に見える。ただし「まったく吸収しない」わけではなく、吸収量が赤や青に比べて圧倒的に少ない、というのが妥当な表現になる。クロロフィルは赤と青を強く吸収する。葉緑素chlorophyllは、赤色(約660 nm) と青色(約430–450 nm) の光を強く吸収する。 これらの光が光合成に最も効率的だからである。緑色光は吸収されにくく、反射・散乱される。クロロフィルは 緑色(約500–550 nm) の光をほとんど吸収しない。そのため反射される。
葉の内部を透過して散乱されることで、私たちの目には葉が緑色に見える。「吸収しない=反射する」ではなく「吸収が少ない=反射・散乱が多い」 、緑色光は完全に無視されているわけではなく、 赤・青に比べて吸収効率が低いため、結果として反射・散乱が優勢になる。 「地球に届く光の中で赤と青が特に豊富で、光合成に適していたため」 という進化的説明も示されている。 さらに、植物はクロロフィル以外にもカロテノイドなどの色素を持つが、これらも緑光をあまり吸収しない。 植物は 赤と青の光を主に吸収して光合成を行う。
緑色光は吸収されにくく、反射・散乱されるため緑に見える。ただし「全く吸収しない」わけではなく、吸収量が少ないだけである。
緑の海がシアノバクテリア繁栄させ、酸素を増加させた。結果、鉄の沈殿(縞状鉄鉱層)に繋がり、さらなる酸素増加による大気の酸化と緑の海は、地球の酸化と生命多様化の原動力となった。
また、緑の海が「生命存在の指標biosignature」になり得る。海に鉄が豊富になれば、光合成生物が酸素を放出し、光の吸収スペクトルを変化させる。惑星の反射光が緑色に偏る可能性があれば、『緑色の海を持つ惑星』として生命活動が進行しているサインかもしれない。
(日本語では生命存在指標ともいうバイオシグニチャーbiosignatureは、惑星を外部から観測したときに、生命が存在する証拠となり得る指標となるデータを指す。通常、惑星大気中に酸素・オゾン・メタンなどの存在を示す証拠が一般的であるが、植物の葉は、葉緑素Chlorophyllによる波長520 nmと680 nm付近の2か所の吸収のために緑色に見える。しかし、実は地上の植物の葉は、赤色750 nm以上の長波長で急激に反射率が立ち上がるという性質を持つことが知られており、レッドエッジと呼ばれている。これは地球のリモートセンシングではすでに利用されているが、仮に太陽系外惑星の表面が植物で覆われている場合にはこのレッドエッジが同定できるかもしれない。そのためこの反射特性は太陽系外惑星探査で重要なバイオシグネチャーとなる可能性が指摘されている。
太陽系内で惑星探査機が惑星現地で行う生命存在確認実験で使用が検討されている蛍光タンパクなどを『生命存在指標』と呼ぶこともある。緑蛍光タンパク質green fluorescent protein(GFP)は、紫外線や青色光を吸収し、より長い波長の光を放出する。この「吸収 → 放出」というプロセスは、生体分子の構造が必要で、非生物的な鉱物では同じスペクトルを出しにくい。 そのため、惑星の反射スペクトルに蛍光特有の【急激な明るさの増加】が見えれば、生命活動の可能性が高まる。)
海に流入した鉄は、太古の海では主に Fe2+(二価鉄イオン)の形で溶けている。二価鉄Fe2+は水中で弱い酸をつくる。Fe2+は水と反応して、次のような平衡を形成する。
Fe2+ + H2O ⇔ FeOH+(ヒドロキソ鉄(II)イオン)+ H+
この反応で 酸性成分の水素イオンH+が放出される。つまり、Fe2+が多いほど、H+ が増えて海水は酸性寄りになる。
酸素が存在する状態では容易に酸化されてFe(OH)3【水酸化鉄(III)】へと変化する。酸化の進行に伴い、淡緑色→灰緑色→黒褐色→赤褐色へと色相が変化する。湿気のある条件下における鉄錆の生成も、一旦2価の鉄イオンFe2+が生じ、空気酸化が進行して3価の水酸化鉄すなわち赤錆となることが知られている。
また、太古の大気には CO2が現在の数百倍〜数千倍あった。そのCO2は海に溶けると炭酸H2CO3をつくる一方、海水を酸性にする。
CO2 + H2O ⇒ H2CO3 ⇒ H+ + HCO3-
この酸性環境は、鉄を Fe2+のまま大量に溶かすのに非常に都合が良い。
つまり、CO2 が多いとH+が増えて海を酸性にする。より鉄が溶けやすくなる。
鉄が更に水H2Oに溶けると、さらに H+を放出して酸性が強まる。という 正のフィードバック が働く。
 |
| 玄武岩を構成する主要ケイ酸塩鉱物の一般式 玄武岩に含まれる ケイ酸塩鉱物そのものに「一つの一般式」はないが、玄武岩を構成する主要鉱物(斜長石・輝石・橄欖石)には、それぞれ 代表的な一般式 が存在する。 斜長石(玄武岩の最も主要な造岩鉱物) アルバイト(NaAlSi3O8) • アノーサイト(CaAl2Si2O8) の固溶体。 輝石(玄武岩の暗色鉱物の中心) 一般式としては、XYSi2O6 (X, Y に Ca, Mg, Fe が入る) 橄欖石(玄武岩の初生鉱物として重要) フォルステライト(Mg2SiO4)とファヤライト(Fe2SiO4)の固溶体。 溶岩流のようにマグマが急冷されてできた玄武岩は結晶化せずにガラス質になることも多い.玄武岩の化学組成は、珪酸(シリカ SiO2)が少なく、鉄やマグネシウムに富んでおり、苦鉄質火山岩に分類される。 玄武岩と同じ組成のマグマがゆっくり冷えて固まると深成岩の斑糲岩になる。 |
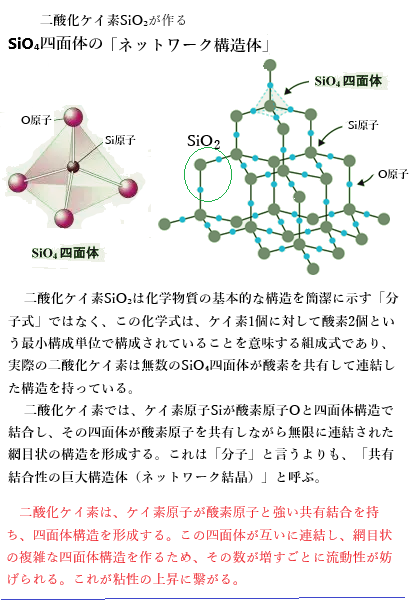
特に玄武岩の風化では、次のような反応で H+が生成 される。玄武岩は主に 輝石pyroxeneや橄欖石olivineなど、 Fe2+・Mg2+を含むケイ酸塩鉱物で構成されている。これらの鉱物は、酸性の水と反応するとH+を放出する方向に反応が進むことがある。また、Fe2+を含む鉱物の風化では H+が生成される。玄武岩の中で特に重要なのは Fe2+を含むケイ酸塩である。これらは風化すると次のような反応を起こす。
太古の海では CO2が極端に多く、また炭酸系との反応が組み合わさるため、結果として H+が増える方向に進む。
Fe2+-珪酸塩silicate + 2H+ ⇒ Fe2+ + 溶解シリカ dissolved silica
(溶解性シリカは、主に水に溶ける形態の二酸化ケイ素SiO2であり、非結晶性シリカとも呼ばれる。)
ここまでは H+を消費するが、その後の Fe2+の酸化で大量の H+が生成される。
太古の海では、シアノバクテリアが放出 した O2によって Fe2+が酸化される。
4Fe2+ + O2 + 4H+ ⇒ 4Fe3+ + 2H2O
さらに Fe3+は水酸化物として沈殿し、その際に H+を放出する。
Fe3+ +3H2O ⇒ Fe(OH)3↓(沈殿)+ 3H+
この 2 つを合わせると、総合反応は、
4Fe2+ + O2 + 1 0H2O ⇒ 4Fe(OH)3↓(沈殿)+ 8H+
つまり、玄武岩が溶けて Fe2+ が海に供給されると、Fe2+が酸化される。結果的に大量の H+が生成され、海が酸性化する。という流れになる。その後の Fe2+の酸化で大量の H+が生成される。
(Fe(OH)3は、.一般に 水酸化鉄(III)【すいさんかてつ・さん】)と呼ばれる。 鉄の酸化数が 3+ のときにできる水酸化物。外観は、赤褐色〜褐色の沈殿として現れる。ゲル状で、乾燥するとより濃い褐色の固体になる 。水にはほとんど溶けない。酸に溶けると、鉄(III)イオン Fe3+を生じる。
Fe(OH)3 +3H+ ⇒ Fe3+ + 3H2O
Fe(OH)3の沈殿生成は pH に強く依存し、 pH が上がるほど沈殿しやすい。そのため、湖沼や湿地の酸化還元状態の変化を読み解く指標にもなる。)
Fe2+含む鉱物 + 4H+ ⇒ e2+ + 溶解成分
風化そのものが酸性化を促すが、酸素がほとんど無かったため、Fe2+が酸化されずに溜まり続けた。
現代の海では、Fe2+はすぐに酸化されて沈殿するが、太古の海は無酸素だったため、Fe2+は酸化されないし、沈殿もしない。海に溶けたまま蓄積するという状態になる。その結果、Fe2+による酸性化が長期間維持された。
酸性=H+が多い環境では、鉄を固体として結びつけている結合が壊されやすくなるからである。鉄を含む鉱物(玄武岩・輝石・角閃石など)は、Fe2+や Feが酸素O2と結びついた結晶構造 を持っている。酸性環境では H+が多いため、次の反応が 起こる。
つまり、H+が鉱物中の O2と結びついて水H2Oを作る。その結果、鉱物の結合が壊れ、Fe2+が溶け出す。これが「酸性だと鉄が溶けやすい」最も基本的な要因となる。鉱物の溶解は一般に、H+が多いほど、反応は右(=溶ける方向)へ進む。というル・シャトリエの原理が働く。太古の大気は CO2が現在の数百〜数千倍。CO2 は海に溶けると、この H+が玄武岩を溶かし、Fe2+を大量に海へ供給する。さらに、玄武岩の風化そのものが H+を消費しながら Fe2+を放出するため、
酸性 → 鉄が溶ける → さらに酸性が維持される
というフィードバックが働く。
太古の海で起きていた『CO2 → 炭酸 → H+→ 玄武岩の溶解 → Fe2+供給』の流れを、代表的な化学反応式で纏めると
まず CO2 が海に溶け、炭酸H2CO3 ・重炭酸HCO3-・H+を生成する。
CO2 + H2O ⇒ H2CO3 ⇒ H+ + HCO3- (この H+が玄武岩【特に Fe2+を含むケイ酸塩鉱物】を溶かす原動力 になる。 )
玄武岩の鉄を代表する鉱物として ファヤライトFe2SiO4(鉄を多く含む橄欖石グループの鉱物)を例にすると、酸による溶解は
Fe2SiO4 + 4H+ ⇒ 2Fe2+ + H4SiO4 (Fe2+は海へ溶け出す鉄 ; H4SiO4は溶存ケイ酸【初期海洋に豊富だった】)
太古代の高 CO2 大気下の 酸性の海は.、玄武岩を急速風化させ、大量の Fe2+が海へ、という流れが当時の地球化学の実体であった。
現代の海は酸素が多いため、Fe2+はすぐに酸化されて沈殿する。しかし太古の海は無酸素で酸性だったため、Fe2+は酸化されにくいためFe(OH)3【鉄(III)水酸化物】のような沈殿物ができにくい、但し海水に溶けて蓄積できる。つまり酸性は「鉄を溶存し、その溶存鉄を保持する」作用に.も働いていた。
③太古代シアノバクテリアの生態
太古代Archean(約40億年前~25億年前)は、「生物層の大転換」、つまり生物圏の劇的な構造変化という意味では、後の原生代に起こる「大酸化イベント(GOE)」ほどの決定的転換は起らなかったが、重要なことは太古代に生命の基盤そのものが形成された。しかも、地球史の中でも極めて重要な『静かな変革』が連続して進行した時代でもあった。太古代の最初期(約40〜38億年前)には、すでに生命が存在した可能性が高い。生命は主に化学合成細菌・古細菌で、熱水環境や浅海で活動していた。これらが地球最初の「生物圏」を形づくった。
太古代の約32〜27億年前のシアノバクテリアは、まだ酸素の乏しい海で、光と鉱物と温泉のような化学エネルギーを頼りに生きていた原核生物であった。最新研究では、当時の海は緑色光が優勢で、シアノバクテリアはその特殊な光環境に適応して進化しし続けた。
大気はほぼ無酸素 、海は鉄イオン(Fe2+)が豊富で緑がかった色をしていた。浅海は紫外線が強く、危険であった。そのため深度数m〜十数mの緑色光が届く層が最適環境であった。太古代の海は、海水に赤色光が吸収されやすく、緑色光が優勢だった。これがシアノバクテリアの光捕集系の進化に影響した。
シアノバクテリアの光合成は、太古代後半に登場したと考えられる。初期段階では、酸素は海中の鉄・硫黄に吸収され、大気にはほとんど放出されてはいない。 つまり、光合成出現の『大規模な革命の種』があっても、まだ「大転換」に至っていない。
太古代は、ヌヴヴアギトゥック・イスア、カープヴァール・ピルバラなどの最古の大陸地殻が形成された時代でもあった。大陸の成長は、浅海域を増やし、微生物マットやストロマトライトの繁栄を支えた。これにより、地球規模の生態系ネットワークが初めて安定化した。
(研究の詳細は2025年6月26日付で科学雑誌『Science』に掲載されているが、カナダ・オタワ大学University of Ottawaはこのほど、同国北東部ケベック州のヌナビク地域にて、地球上で確認されている中でも最古の岩石を発見したと発表した。 その年代は冥王代【約46〜40億年前】の約41億6000万年前、これは地球が誕生したとされる約45.4億年前にごく近い時期、地球の創世期、冥王代に形成された岩石であることが判明した。
ヌナビク地域に広がる「ヌヴヴアギトゥク・グリーンストーン帯Nuvvuagittuq Greenstone」は、長年、地質学者たちの注目を集めてきた地域であった。 ここでは数十億年前の岩石が地表に露出しており、「地球最古の岩石が眠っているかもしれない」と期待されていた。
オタワ大学の地質学者クリスチャン・ソール氏を中心とする研究チームは、ウラン-鉛法とサマリウム-ネオジム法という2種類の放射年代測定法を同時に適用し、その結果、異なる鉱物・異なる採取地点においても、共通して41.6億年前という驚くべき年代が示された。)
太古代のシアノバクテリアは、現代のような高度な光捕集系のアンテナ複合体フィコビリソームphycobilisomeを持つ前段階にあった。やがて、緑色光を効率よく吸収する色素構造を進化させたが、未だ酸素発生型光合成の効率は低かった。初期のシアノバクテリアは、光だけでなく周囲の化学エネルギーも利用していた。鉄イオン(Fe2+)の酸化 • 硫黄化合物の利用 • 温泉・海底熱水噴出孔周辺での化学合成的生活など、光が弱い環境では、化学エネルギーが重要な補助源であった。それでも光合成の副産物として酸素を微量に放出し始めていた。この酸素が数億年かけて蓄積し、約24億年前の原生代初期の大酸化イベントGreat Oxidation Event(GOE)に繋がった。
シアノバクテリアは粘液を分泌し、砂粒や炭酸塩を捕捉して層状構造を作った。ストロマトライトstromatoliteは太古代のシアノバクテリア群集の痕跡は、3.5億年前の西オーストラリア・ピルバラのものが有名で、 微生物マットの都市のような構造で、多様な微生物が共存していた痕跡でもあった。
ストロマトライトは、シアノバクテリアが光合成を行う際に、死骸や生成された炭酸カルシウムの沈殿が、層を作ることで形成された。この過程は太古代の中期の約35億年前から始まったと考えられている。ストロマトライトは、層状の構造を持ち、シアノバクテリアの活動によって作られた堆積物が積み重なったもので、これにより、初期の地球の生命活動を示す重要な化石となっている。ストロマトライトは、初期の酸素生成の証拠であり、地球の酸素供給の最初の兆しを示す。これにより、古代の地球環境の変化に関する重要な手がかりを提供した。
シアノバクテリアの生態は、地球史を根本から変えた。光合成で生じた酸素が海中の鉄を酸化し、縞状鉄鉱層Banded Iron Formation(BIF)を形成した。縞状鉄鉱層は、シアノバクテリアが生成した酸素が、海水中の鉄イオンを酸化して酸化鉄を形成する過程で作られた。この反応は、原生代前期の約20億年前の酸素が少ない環境で起こった。この縞状鉄鉱層は、酸化鉄を主体とする堆積鉱床であり、鉄鉱石の鉱床として世界中に非常に大規模に形成された。これらが、鉄鉱石の主要な供給源となった。
縞状鉄鉱層は、酸素の放出が地球の環境に与えた影響を示す証拠であり、地球の酸素化を示す重要な資料となった。これにより、初期の酸素革命が生命と環境に与えた影響を理解するための貴重な情報を提供する。海水中の鉄イオン(Fe2+)が枯渇すると、酸素が大気へ蓄積し、やがて約24億年前に大酸化イベント(GOE)が発生 • これが真核生物・多細胞生物の進化の前提条件となった。
「大転換」は、太古代の後、原生代初期の約24億年前に起きた大酸化イベント(GOE)を契機とする。大気中の酸素濃度が急上昇しメタン温室効果が崩壊 した。その後に、全球凍結Snowball Earth • 好気呼吸の進化 • 真核生物の登場などの土台が整う。つまり、太古代はGOEという大転換の準備期間だった。
目次へ